村上定瞭(水浄化フォーラム)
1.酸化還元反応と自由エネルギー
酸化還元反応は、物質間での電子の移動反応である。今、つぎの反応を例に挙げる。
A(e-donor) + B(e-recepter) = A+ + B– (1)
反応(1)は、式(2)と(3)に分解できる。
A = A+ + e– (2)
B + e– = B– (3)
ところで、物質Xの自由エネルギーGXは、次式で示される。
GX = μX
μX = μ°X + RT ln aX
(μX:化学ポテンシャル、aX:活量)
式(1)の反応の自由エネルギー変化ΔGは、
ΔG = Gright – Gleft
= GA+ + GB+ – GA -GB
= ΔG°+ RTln K
K = aA+·aB–/(aA·aB)
今、化学反応はΔGが減少する方向へ進行するので、反応式(1)において、
① Gleft > Grightならば右方向へ反応が進行する。
② Gleft < Grightならば左方向へ反応が進行する。
しかしながら、Gleftに外部エネルギーGoutが加わり、Gleft + Gout > Grightとなれば、右方向へ反応が進行することとなる。
反応(1)は、式(2)と(3)に分解できる。
B + e– = B– (3)
ところで、物質Xの自由エネルギーGXは、次式で示される。
μX = μ°X + RT ln aX
(μX:化学ポテンシャル、aX:活量)
式(1)の反応の自由エネルギー変化ΔGは、
= GA+ + GB+ – GA -GB
= ΔG°+ RTln K
K = aA+·aB–/(aA·aB)
今、化学反応はΔGが減少する方向へ進行するので、反応式(1)において、
① Gleft > Grightならば右方向へ反応が進行する。
② Gleft < Grightならば左方向へ反応が進行する。
しかしながら、Gleftに外部エネルギーGoutが加わり、Gleft + Gout > Grightとなれば、右方向へ反応が進行することとなる。
2.自然界における酸化還元反応の事例
(1)光合成(生産)と酸素呼吸(消費)
光合成の一つとして、炭酸CO2と水H2Oが(太陽)光エネルギーを受けて炭水化物CH2Oを生成する反応がある。この反応は複雑な生物学的反応で構成されているが、簡略化するとつぎのように示される。この反応では、CO2のC(+4)がCH2OではC(±0)となり、Cは還元されている。
CO2 + H2O + hν(光エネルギー) = CH2O + O2
C(+4 in CO2) + 4e– = C(±0 in CH2O)
2O(-2 in CO2) = 2O(±0 in O2) + 4e–
酸素呼吸は、上記反応が右から左へ進行する反応で、Cは酸化されている。この反応で発生するエネルギーは化学エネルギー物質(ATPなど)へ変換され、細胞内での様々な反応を進行させるエネルギー源Goutとなっている。
(2)金属材料の腐食(さび)
金属元素の多くは、自然界では酸化物・硫化物として存在し、金属材料は様々な方法(製錬)によって酸化や還元されて生産される。
ところが、金属材料は、酸素が存在する環境では酸化物の状態が安定である。酸素との直接反応は常温ではなかなか進行しないが、水分が付着するか中性の水中では、金属は酸化されて、さび(腐食)が発生する。図1にそのメカニズムを示す。鉄片を水中に浸すと、その表面の環境条件は均一ではなく、ある点(灰色の○:正極)と離れたある点(薄赤の○:負極)の間で濃淡電池が形成され、負極ではFeが2e–を放出してFe2+となる。正極では、O2/2がFe片内を移動してきた2e-を受け取り、O2-(酸素イオン:鉄表面でFe-O2--Fe)が生成し、直ちにO2-はH2Oと反応して2OH–へ変化する。
負極で生じたFe2+は酸性溶液では溶出・溶解するが、中性では不溶性の水酸化鉄(Ⅱ)Fe(OH)2となり、負極点に留まる。この一部はさらに酸化されて、FeO(OH)で示される赤さびとなる。
このように、酸素が電子が受容体となり、金属材料は腐食が進行し、金属部分が減少して構造物の破損の原因となる。電解質が共存すると腐食が促進され、淡水よりも海水で腐食速度は速くなる。
C(+4 in CO2) + 4e– = C(±0 in CH2O)
2O(-2 in CO2) = 2O(±0 in O2) + 4e–
酸素呼吸は、上記反応が右から左へ進行する反応で、Cは酸化されている。この反応で発生するエネルギーは化学エネルギー物質(ATPなど)へ変換され、細胞内での様々な反応を進行させるエネルギー源Goutとなっている。
ところが、金属材料は、酸素が存在する環境では酸化物の状態が安定である。酸素との直接反応は常温ではなかなか進行しないが、水分が付着するか中性の水中では、金属は酸化されて、さび(腐食)が発生する。図1にそのメカニズムを示す。鉄片を水中に浸すと、その表面の環境条件は均一ではなく、ある点(灰色の○:正極)と離れたある点(薄赤の○:負極)の間で濃淡電池が形成され、負極ではFeが2e–を放出してFe2+となる。正極では、O2/2がFe片内を移動してきた2e-を受け取り、O2-(酸素イオン:鉄表面でFe-O2--Fe)が生成し、直ちにO2-はH2Oと反応して2OH–へ変化する。
負極で生じたFe2+は酸性溶液では溶出・溶解するが、中性では不溶性の水酸化鉄(Ⅱ)Fe(OH)2となり、負極点に留まる。この一部はさらに酸化されて、FeO(OH)で示される赤さびとなる。
このように、酸素が電子が受容体となり、金属材料は腐食が進行し、金属部分が減少して構造物の破損の原因となる。電解質が共存すると腐食が促進され、淡水よりも海水で腐食速度は速くなる。
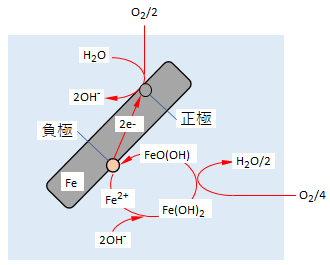
図1 中性の水中における鉄片の腐食(さび)の発生メカニズム
3.水浄化と酸化還元反応
水には様々な溶質や微細な固形物質が含まれており、用水・排水の処理において、これらの物質を分離・除去する際に、酸化還元プロセスは重要な手法の一つであるとともに、生物学的プロセスにおいても重要な制御因子となる。
<金属の製法>
例えば、Feは溶鉱炉の中で、磁鉄鉱F3O4や赤鉄鉱F2O3にコークスCと石灰CaCO3を加えて熱風を送り、高温で還元して、銑鉄(Cを4%程度含む)を得る。銑鉄は転炉で酸素を吹き込み、不純物やCを除いて鋼(C:0.02~2%)とする。
Cuは、主に黄銅鉱CuFeS2を原料とし、コークスと石灰を溶鉱炉で加熱し、Fe2O3とCu2Sに分解し、融解したCu2Sを転炉で酸素を吹き込み、粗銅Cuを得る。この粗銅を陽極(溶解)、純銅を陰極(析出)にして電気分解し、肥大化した陰極を取り出してCu材料としている。
掲載日:2018年01年24日
更新日:
Cuは、主に黄銅鉱CuFeS2を原料とし、コークスと石灰を溶鉱炉で加熱し、Fe2O3とCu2Sに分解し、融解したCu2Sを転炉で酸素を吹き込み、粗銅Cuを得る。この粗銅を陽極(溶解)、純銅を陰極(析出)にして電気分解し、肥大化した陰極を取り出してCu材料としている。
