Outline and Planning of Genetic Testing
村上定瞭(水浄化フォーラム), Sadaaki Murakami (Water & Solutions Forum)
1.検査室の環境
2.検査に必要な機器
2.1 専門機器
2.2 一般機器
3.検査に必要な機材
4.検査に必要な試薬・酵素
5.検査に用いる主な酵素
5.1 DNA合成酵素
5.2 逆転写酵素
5.3 核酸加水分解酵素
遺伝子検査-略語一覧
参考文献
1. Laboratory environment
2. Equipment required for testing
2.1 Specific equipment
2.2 General equipment
3. Apparatus required for testing
4. Reagents and enzymes required for testing
5. Main enzymes used for testing
5.1 DNA synthases
5.2 Reverse transcriptase
5.3 Nucleic acid hydrolases
Abbreviations list of genetic testing
References
(1) 遺伝子検査を行う際にはコンタミネーションを防止することが重要であるため検査室の環境を整えておく必要がある。
(2) 遺伝子検査に使用する機器は、一般機器から専用機器など多岐にわたるため、使用目的に合わせた正しい使い方をする。
(3) 各試薬メーカーから多種多様の抽出キットや機器、機材が販売されているので購入時には必要に応じて十分な検討が必要である。
(1) Since it is important to prevent contamination when conducting genetic tests, it is necessary to prepare the environment of the laboratory.
(2) Since the equipments used for genetic testing ranges from general equipments to dedicated equipment, use them correctly according to the purpose of use.
(3) Since a wide variety of extraction kits, equipments, and equipments are sold by each reagent manufacturer, it is necessary to carefully consider them as necessary at the time of purchase.
1.検査室の環境
遺伝子検査は、検体の全処理から遺伝子解析まで、多くの工程から構成される。
PCR法は、非常に高感度な検出方法であり、RNA分子は、非常に不安定なため取扱いには特に注意が必要である。RNAはRNA分解酵素(RNase)により容易に分解され、このRNaseは検査材料(血液、骨髄液、尿、組織など)、検査機器、試薬、さらに検査従事者の唾液や汗からも混入することがあり、細心の注意が必要となる。本項では、遺伝子検査に必要な環境設備、機器、機材を取り上げる。
1. Laboratory environment
Genetic testing consists of many steps, from complete sample processing to genetic analysis.
The PCR method is a very sensitive detection method, and RNA molecules are extremely unstable, so special care must be taken when handling them. RNA is easily degraded by RNA-degrading enzymes (RNases), which can be contaminated with test materials (blood, bone marrow, urine, tissues, etc.), testing equipment, reagents, and even saliva and sweat of testers. Yes, you need to be very careful. This section covers the environmental equipment, equipment, and equipment required for genetic testing.
1.1 作業エリアの区分
PCR検査を行う環境は、コンタミネーションを防止することを主目的として、4つのエリアを設けることが理想である。
・エリア1: 試薬調整、分注エリア
・エリア2: 核酸抽出エリア
・エリア3: 遺伝子増幅装置およびその産物を取り扱うエリア
・エリア4: 電気泳動エリア
(1) クリーンベンチ・安全キャビネット
クリーンベンチは、クロスコンタミネーション、キャリーオーバーコンタミネーションの防止や、核酸分解酵素の混入を回避する目的で、核酸抽出エリアとして使用できる。また、外部からのコンタミネーションを防ぎ清潔区域として利用され、PCR試薬調整に利用することもできる。
検体の前処理や細胞破砕などは、感染物質の飛散を防止するために安全キャビネット中で行うことが適切である。安全キャビネットは、装置の機能と構造により分類され、遺伝子組換え生物や病原体などのバイオバザー物質を封じ込めるための装置であるため、取り扱う病原体(特にM. tuberculossis)によって取扱いやバイオセーフティー指針が定められている。
(表1 バイオセーフティー指針)
1) 各エリアで使用する機器、機材などはエリアごとに用意し、共通使用は避ける。
2) 検査従事者は、RNaseの混人を防ぐため、作業中は清潔なマスク、パウダーフリー手袋を着用する。また鋳型となるDNAが存在しないように注意する必要がある。
3) 検査室内の作業台、使用機器は、作業前後に次亜塩素酸ナトリウム溶液で清拭し常に清潔に保つ。作業中に汚染を認めた場合には次亜塩素酸ナトリウム溶液で清掃し、70%エタノール溶液で拭き取る。
1.1 Work area division
Ideally, the environment for performing the PCR test should have four areas with the main purpose of preventing contamination.
・ Area 1: Reagent adjustment and dispensing area
・ Area 2: Nucleic acid extraction area
・ Area 3: Area where gene amplification devices and their products are handled
・ Area 4: Electrophoresis area
(1) Clean bench / safety cabinet
The clean bench can be used as a nucleic acid extraction area for the purpose of preventing cross-contamination and carry-over contamination and avoiding contamination with nucleic acid-degrading enzymes. In addition, it is used as a clean area to prevent contamination from the outside, and can also be used for PCR reagent adjustment.
It is appropriate to perform sample pretreatment and cell crushing in a safety cabinet to prevent the scattering of infectious substances. Safety cabinets are classified according to the function and structure of the device, and are devices for containing biohazard substances such as genetically modified organisms and pathogens (especially M. tuberculossis, etc.).
(Table 1 Biosafety Guidelines)
1) Prepare equipment and equipment for each area and avoid common use.
2) Testers should wear clean masks and powder-free gloves during work to prevent RNase contamination. It is also necessary to be careful that there is no template DNA.
3) The work table and equipment used in the testing room should be wiped with sodium hypochlorite solution before and after work to keep them clean at all times. If contamination is found during work, clean with sodium hypochlorite solution and wipe with 70% ethanol solution.

写真1.1 クリーンベンチ
https://www.monotaro.com/g/04548602/#

写真1.2 安全キャビネット
https://www.airtech.co.jp/products/cleanbench/1044/
2.検査に必要な機器
2.1 専門機器
(1) 核酸増幅装置(サーマルサイクラー、PCR装置)
温度サイクルおよびインキュベート時間を自動制御する、PCR用の装置で逆転写反応、PCR反応に用いられる。
(2) リアルタイムPCR解析システム
サーマルサイクラーを発展させPCR増幅装置と分光蛍光光度計を一体化した装置で、PCR増幅産物をサイクルごとにリアルタイムに検出する。
(3) デジタルPCR解析システム
内部標準や内因性コントロールに頼らず、標的分子数を直接カウントするので、従来のリアルタイム定量PCR法に代わって絶対定量や希少対立遺伝子などの検出を行うことができる装置である。
(4) DNAシーケンサー
① キャピラリーDNAシーケンサー
サイクルシーケンス法、ジデオキシ法を原理として、遺伝子解析、多型解析に用いられている。
② 次世代シーケンサー
全ゲノム、全エクソン領域を対象とした解析を行う。最近では、小型次世代シーケンサーが各社より開発・販売されている。
(5) 核酸自動抽出装置
各メーカーより核酸吸着媒体に多孔質メンブレンを使用した高速・高純度・高収量の自動核酸分離システムが発売されている。
(6) 分光光度計
抽出された核酸の濃度測定を行う。キュベットを使用せずに1~2μLの核酸溶液で短時間に測定可能な装置が販売されている。
(7) 電気泳動装置
① アガロースゲル電気泳動装置
アガロースゲル(0.5~4%)を用いて核酸の電気泳動を行う。
② ポリアクリルアミドゲル電気泳動装置
ポリアクリルアミドゲル(3.5~20%)を用いて核酸の電気泳動(PAGE)を行う。とくに100bp以下の短いPCR産物やオリゴヌクレオチドの確認に適している。スラブ型電気泳動装置を使用するには電気泳動用の電源装置が必要になる。
③ キャピラリー電気泳動装置
内径20~100μm以下、長さ30~50cmの毛細管内で電気泳動を行う装置。自動塩基配列解析装置(DNAシーケンサー)に応用されている。
④ パルスフィールドゲル電気泳動装置
巨大DNA断片(50kbp~10Mbp)の電気泳動を行う。ヒトや種々の微生物のゲノム解析に用いられ、院内感染ルートの原因菌解明などに利用されている。
(8) 電気泳動撮影装置
トランスイルミネーターで紫外線を照射し、電気泳動後のゲル内のエチジウムブロマイド(EtBr)を蛍光励起して核酸を検出する。CCDカメラやデジタルカメラ付きの両像取込装置がある。
2. Equipment required for testing
2.1 Specific equipment
(1) Nucleic acid amplification device (thermal cycler, PCR device)
Used for reverse transcription reaction and PCR reaction in a PCR device that automatically controls the temperature cycle and incubation time.
(2) Real-time PCR analysis system
A device that integrates a PCR amplification device and a spectral fluorometer by developing a thermal cycler, and detects PCR amplification products in real time on a cycle-by-cycle basis.
(3) Digital PCR analysis system
Since the number of target molecules is directly counted without relying on internal standards or endogenous controls, it is a device that can perform absolute quantification and detection of rare alleles instead of the conventional real-time quantitative PCR method.
(4) DNA sequencer
① Capillary DNA sequencer
It is used for gene analysis and polymorphism analysis based on the & emsp; cycle sequencing method and dideoxy method.
② Next-generation sequencer
Perform analysis for the entire genome and all exon regions. Recently, small next-generation sequencers have been developed and sold by various companies.
(5) Nucleic acid automatic extractor
Each manufacturer has released a high-speed, high-purity, high-yield automatic nucleic acid separation system using a porous membrane as a nucleic acid adsorption medium.
(6) Spectrophotometer
Measure the concentration of the extracted nucleic acid. Devices that can measure in a short time with 1 to 2 μL of nucleic acid solution without using a cuvette are on the market.
(7) Electrophoresis device
① Agarose gel electrophoresis device
Nucleic acid electrophoresis is performed using an agarose gel (0.5~4%).
② Polyacrylamide gel electrophoresis device
Perform nucleic acid electrophoresis (PAGE) using polyacrylamide gel (3.5-20%). Especially suitable for confirmation of short PCR products and oligonucleotides of 100 bp or less. To use the slab type electrophoresis device, a power supply device for electrophoresis is required.
③ Capillary electrophoresis device
A device that performs electrophoresis in a capillary tube with an inner diameter of 20 to 100 μm or less and a length of 30 to 50 cm. It is applied to an automatic base sequence analyzer (DNA sequencer).
④ Pulsed field gel electrophoresis device
Perform electrophoresis of a large DNA fragment (50kbp ~ 10Mbp). It is used for genome analysis of humans and various microorganisms, and is used for elucidating the causative bacteria of nosocomial infection routes.
(8) Electrophoresis imaging device
The nucleic acid is detected by irradiating ultraviolet rays with a transilluminator and fluorescently exciting ethidium bromide (EtBr) in the gel after electrophoresis. There are both image capture devices with a CCD camera and a digital camera.

写真2.1.1 サーマルサイクラー
https://www.wakenyaku.co.jp/ctg/det.php?i=758

写真2.1.2 リアルタイムPCR解析システム
https://www.wakenyaku.co.jp/ctg/det.php?i=753

写真2.1.3 デジタルPCR解析システム
https://www.wakenyaku.co.jp/ctg/det.php?i=751

写真2.1.4 DNAシーケンサー
https://www.wakenyaku.co.jp/ctg/det.php?i=743

写真2.1.5 次世代シーケンサー
https://jp.illumina.com/systems/sequencing-
platforms/nextseq.html
2.2 一般機器
(1) ボルテックスミキサー
試薬の溶解、混和、撹伴に使用し、均一化するとtokutei
きに用する。
(2) 遠心機
① 低速遠心機
最高遠心力およそ2、000~2、600g(最高回転は4、000~5、000rpm)の範囲で、血液から単核細胞層を回収するときや細胞の沈澄を得るときに使用する。
② 高速遠心機
最高遠心力およそ15,000~19,000g(最高回転数は15,000rpm)で、マイクロチューブを使用した核酸抽出時に使用する。
③ 小型微量遠心機
最高遠心力2,000g(最高回転数は約6,000~10,000rpm)で、マイクロチューブ(1.5mLチューブ用、PCRチューブ用)内の試薬をスピンダウンするときに使用する。
(3)高圧蒸気滅菌器(オートクレーブ)
マイクロチューブやピペットチップなどのプラスチック製品や液体の滅菌に使用する。試薬や器具類の滅菌用と生物学的汚染物質の滅菌用とは区別する必要がある。
(4) 恒温水槽・恒温器
① 温度可変式ピートブロック
金属のブロックにマイクロチューブを差し込んで一定温度を保つ装置で、遺伝子検査ではよく用いられている。
② 恒温水槽
ウォーターバスともいわれ、一定温度の湯の中にチューブを浸けて温度を保つ装置で、37℃・1時問などの酵素反応などに用いられる。チューブ周りについた水などがチューブ内に入ることがあるので、注意する。
③ 恒温器
インキュベーターともいわれ、内部の空気の温度を一定に保つ装置で、長時間のインキュベーションに用いられる。
(5) 電子天秤
自家調整試薬の秤量に使用する。
(6) 純水製造装置
自家調整試薬には精製水を使用する。電気泳動用バッファ一には精製されたイオン交換水または逆浸透(RO)水を使用する。
(7) 冷凍・冷蔵庫
検体採取後は、目的や材料によって低温保存(4℃)、または必要に応じて凍結保存(-80℃)する。またPCR法で使用する酵素などの試薬は、冷凍保存(-20℃)など試薬の保存管理が重要になるため、各種目的に合わせた冷凍・冷蔵庫が必要である。
2.2 General equipment
(1) Vortex mixer
Used for dissolving, mixing and stirring reagents, and for homogenization.
(2) Centrifuge
① Low speed centrifuge
Used when recovering mononuclear cell layers from blood or obtaining cell clarification in the range of maximum centrifugal force of about 2,000 to 2,600 g (maximum rotation is 4,000 to 5,000 rpm). ..
② High-speed centrifuge
Maximum centrifugal force of approximately 15,000-19,000 g (maximum rotation speed of 15,000 rpm), used during nucleic acid extraction using microtubes.
③ Small micro centrifuge
Used when spinning down reagents in microtubes (for 1.5 mL tubes, PCR tubes) with a maximum centrifugal force of 2,000 g (maximum rotation speed is about 6,000 to 10,000 rpm).
(3) High pressure steam sterilizer (autoclave)
Used for sterilization of plastic products and liquids such as microtubes and pipette tips. It is necessary to distinguish between the sterilization of reagents and equipment and the sterilization of biological contaminants.
(4) Incubator / Incubator
① Variable temperature Pete block
A device that maintains a constant temperature by inserting a microtube into a metal block, which is often used in genetic testing.
② Constant temperature water bath
Also known as a water bath, it is a device that maintains the temperature by immersing a tube in hot water at a constant temperature, and is used for enzymatic reactions such as 37 ° C and 1 hour. Be careful as water around the tube may get inside the tube.
③ Incubator
Also known as an incubator, it is a device that keeps the temperature of the air inside constant and is used for long-term incubation.
(5) Electronic balance
Used for weighing self-adjusting reagents.
(6) Pure water production equipment
Purified water is used as the self-adjusting reagent. Purified ion-exchanged water or reverse osmosis (RO) water is used for the electrophoresis buffer.
(7) Freezer / refrigerator
After collecting the sample, store it at a low temperature (4℃) depending on the purpose and material, or freeze it (-80℃) if necessary. For reagents such as enzymes used in the PCR method, storage management of reagents such as frozen storage (-20℃) is important, so it is necessary to have a freezer / refrigerator suitable for various purposes.
3.検査に必要な機材
(1) マイクロピペット
試薬などの分取などに使用し、扱う液量に応じて適切なものを使用する(0.5~10μL、10μL~100μL、100~1,000μL)。
(2) ピペットチップ
コンタミネーション防止のためフィルター付きチップを使用し、使用するマイクロピペットに合ったチップを用いる。
(3) マルチピペット
PCR試薬などを連続分注時に使用する。
(4) チューブ関連
チューブの素材はポリプロピレン製を推奨する。ヌクレアーゼフリーで滅菌済みのものを使用する。
① 50mL、15mL、5mLスクリューキャップチューブ
試薬分注や調整に使用する。
② 1.5mL、2.0mLチューブ
核酸抽出用に主に使用する。
③ PCR用0.2mLチューブ
PCR用のチューブとして使用する。
(5) トランスファーピペット、1mLスポイト
エアロゾル防止のため先の細いもの(滅菌済み)を使用し、使い捨てとする。
(6) マイクロプレート 96穴用(縦8個×横12個)、ウェルラック
PCR用チューブとして多検体を処理する時などに使用する。
(7) ホモジナイザー
核酸抽出時の組織のホモジナイズに使用する。使い捨て型のホモジナイザー(バイオマッシャー)は時間と手間が掛からず効果的に試料を破砕することができる。
3. Apparatus required for testing
(1) Micropipette
Used for sorting reagents, etc., and use the appropriate one according to the amount of liquid to be handled (0.5 to 10 μL, 10 μL to 100 μL, 100 to 1,000 μL).
(2) Pipette tip
Use a tip with a filter to prevent contamination, and use a tip that matches the micropipette used.
(3) Multi-pipette
Use PCR reagents, etc. during continuous dispensing.
(4) Tube related
The material of the tube is recommended to be polypropylene. Use nuclease-free and sterilized ones.
① 50mL, 15mL, 5mL screw cap tube
Used for reagent dispensing and adjustment.
② 1.5mL, 2.0mL tube
Mainly used for nucleic acid extraction.
③ 0.2mL tube for PCR
Used as a tube for PCR.
(5) Transfer pipette, 1mL dropper
Use a fine-tipped object (sterilized) to prevent aerosols and make it disposable.
(6) Microplate for 96 holes (8 vertical x 12 horizontal), well rack
Used as a PCR tube when processing multiple samples.
(7) Homogenizer
Used for tissue homogenization during nucleic acid extraction. The disposable homogenizer (biomasher) can effectively crush the sample without taking time and effort.
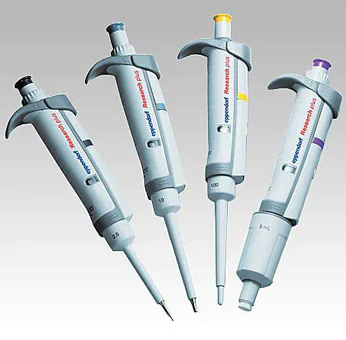
写真3.1 マイクロピペット
https://www.monotaro.com/g/01372332/#

写真3.2 フィルターチップ
https://www.monotaro.com/g/01362054/#

写真3.4 ディスポーザブルホモジナイザー
https://axel.as-1.co.jp/asone/d/2-3869-01/
4.検査に実用な試薬・酵素
(1) バッファ一関連試薬
① DNaseフリー、RNaseフリー水(精製水)
DNAやRNAサンプルの溶解などに使用する。
② 0.1%ジエチルピロカーボネート(DEPC)処理水
DEPCは、RNase阻害効果があるためRNAを取り扱う際に使用する。発がん性が疑われるため取扱いに注意する。
③ TEバッファー(pH 8.0)
Tris溶液(pH 8.0)とEDTA溶液(pH8.0)を混合しオートクレーブ処理したもの。TEバッファ一に含まれるEDTAは2価の金属イオンのキレート剤で、Mg2+に結合して、核酸分解酵素(DNase)のはたらきを弱める効果がある。また、pHを弱アルカリ性にすることで、DNAやRNAの沈殿と分解を防ぐはたらきもある。
④ 0.5mol/L EDTA溶液(pH 8.0)
⑤ 1mol/Lトリス塩酸バッファー(Tris-HCl)
⑥ トリス緩衝生理食塩水(TBS Buffer)
⑦ リン酸バッファー(PBS buffer)
⑧ トリス・グリシン泳動バッファー(TG-SDS buffer)
⑨ SSCバッファー(SSC buffer)
(2) 抽出関連試薬
① 抽出キット(RNA、DNA)
各試薬メーカーから抽出キットが販売されており、DNA抽出法は凝集分配法やスピンカラム法にもとづいたキットがある。 RNA抽出法には、AGPC法とスピンカラム法にもとづいたキットがある。
② lysis buffer(細胞溶解液)
③ クロロホルム特級
④ 2-プロパノール特級(イソプロピルアルコール
⑤ 70%エタノール溶液
(3) 酵素試薬
① 逆転写酵素(cDNA合成酵素)
② 耐熱性DNAポリメラーゼ
③ 制限酵素
(4) 泳動関連試薬
① 50x TAE buffer(トリス・酢酸・EDTA)
② 10x TBE buffer(トリス・ホウ酸・EDTA)
③ 10x Tris-glydne buffer(トリス・グリシン)
④ アガロースゲル、ポリアクリルアミドゲル
ゲル電気泳動に使用するアガロースは、寒天を高度に精製しアガロベクチンを除いたもので、数百bp~数十kbpの分子量の大きい核酸を分離するのに使用する。また、ポリアクリルアミドゲルは、PAGEの担体として使用され。アガロースゲルよりも網日が細かいため10bp~数百bpの短い核酸の分離に使川する。アクリルアミドは、皮膚や粘膜から吸収されると神経毒となるため、取扱いに注意する。
⑤ 分子量マーカー(DNAラダーマーカー)
各分子量範囲に適応した電気泳動用の分子量マーカーを選択して使用する。
⑥ ローディングバッファー
電気泳動用核酸サンプルを調製する際に添加する試薬である。ローディングバッファーには、アプライの際にウェル(ゲルの穴)の中にDNAサンプルが沈むように比重を増やすためのグリセロール、またフィコールなど電気泳動の進行を観察できる色素が含まれる。
⑦ EtBr液
二本鎖DNAの鎖の間に入り込む単光試薬で発がん作用と毒性があるので、取扱いには必ず手袋を着用する。EtBr廃液は必ず次亜塩素酸で中和処理をしてから捨てる。
(5) PCR関連試薬
① 定性検査
・超純水
・PCRバッファー
・デオキシリボヌクレオシド三リン酸(dNTP)混合液
・塩化マグネシウム
・プライマー
・Taq DNAポリメラーゼ
② 定量検査
・超純水
・マスターミックス
・DNAプライマー
・プローブ
・蛍光DNA結合色素(SYBR® Green I 色素など)
4. Reagents / enzymes practical for testing
(1) Buffer related reagents
① DNase-free, RNase-free water (purified water)
Used for lysis of DNA and RNA samples.
② 0.1% Dethylpyrocarbonate (DEPC) treated water
DEPC is used when handling RNA because it has an RNase inhibitory effect. Handle with care as it is suspected to be carcinogenic.
③ TE buffer (pH 8.0)
Tris solution (pH 8.0) and EDTA solution (pH 8.0) are mixed and autoclaved. EDTA contained in TE buffer is a chelating agent for divalent metal ions, which has the effect of binding to Mg2+ and weakening the function of nucleic acid degrading enzyme (DNase). It also has the function of preventing the precipitation and degradation of DNA and RNA by making the pH weakly alkaline.
④ 0.5mol / L EDTA solution (pH 8.0)
⑤ 1 mol / L Tris-HCl buffer (Tris-HCl)
⑥ Tris buffered saline (TBS Buffer)
⑦ Phosphate buffer (PBS buffer)
⑧ Tris-glycine migration buffer (TG-SDS buffer)
⑨ SSC buffer
(2) Extraction-related reagents
① Extraction kit (RNA, DNA)
Extraction kits are sold by each reagent manufacturer, and there are kits based on the aggregation and distribution method and the spin column method as the DNA extraction method. RNA extraction methods include kits based on the AGPC method and the spin column method.
② lysis buffer (cell lysate)
③ Chloroform special grade
④ 2-Propanol special grade (isopropyl alcohol)
⑤ 70% ethanol solution
(3) Enzyme reagent
① Reverse transcriptase (cDNA synthase)
② Thermostable DNA polymerase
③ Restriction enzymes
(4) Reagents related to electrophoresis
① 50x TAE buffer (Tris, acetic acid, EDTA)
② 10x TBE buffer (Tris / boric acid / EDTA)
③ 10x Tris-glydne buffer
④ Agarose gel, polyacrylamide gel
Agarose used for gel electrophoresis is a highly purified agar from which agarobectin has been removed, and is used to separate nucleic acids with a large molecular weight of several hundred bp to several tens of kbp. Polyacrylamide gel is also used as a carrier for PAGE. Since the net day is finer than that of agarose gel, it is used for separating short nucleic acids of 10 bp to several hundred bp. Acrylamide becomes a neurotoxin when absorbed through the skin and mucous membranes, so handle with care.
⑤ Molecular weight marker (DNA ladder marker)
Select and use a molecular weight marker for electrophoresis suitable for each molecular weight range.
⑥ Loading buffer
A reagent added when preparing nucleic acid samples for electrophoresis. The loading buffer contains glycerol to increase the specific gravity so that the DNA sample sinks into the wells (gel holes) during application, and dyes such as Ficoll that allow observation of the progress of electrophoresis.
⑦ EtBr liquid
A monoluminous reagent that enters between the strands of double-stranded DNA and is carcinogenic and toxic, so be sure to wear gloves when handling. Be sure to neutralize the EtBr waste liquid with hypochlorous acid before discarding it.
(5) PCR-related reagents
① Qualitative test
・ Ultrapure water
・ PCR buffer
・ Deoxyribonucleoside triphosphate (dNTP) mixture
・ Magnesium chloride
・ Primer
・ Taq DNA polymerase
② Quantitative test
・ Ultrapure water
・ Master mix
・ DNA primer
・ probe
・ Fluorescent DNA binding dye (SYBR® Green I dye, etc.)
5.検査に用いる主な酵素
DNA合成酵素は、一本鎖の核酸を鋳型として、それに相補的な塩基配列をもつDNA鎖を合成する酵素の総称である。DNAを鋳型としてDNAを合成するDNA依存性DNAポリメラーゼと、RNAを鋳型としてDNAを合成するRNA依存性DNAポリメラーゼの2つのタイプがある。
DNA合成酵素は、さまざまな種類が存在するので、PCR検査を行う場合にはそれぞれの特徴を理解した上で、検査に必要な酵素を選ぶ必要がある。
5.1 DNA合成酵素(DNAポリメラーゼ)
DNA合成酵素は、鋳型となる一本鎖DNAに相補的なdNTPを娘鎖の3’末端に結合し、鎖を延長する酵素の総称である。この酵素は、3’→5’方向にDNA親鎖を読み取り、5’→3’方向に親鎖に相補的な新しい鎖(娘鎖)を延長して2本鎖DNAを合成する。ポリメラーゼの基質は、4種類のデオキシリボヌクレオシド三リン酸(dATP、dGTP、dCTP、dTTP)である。DNA依存性DNAポリメラーゼは、DNA複製とDNA修復において中心的な役割を果たす酵素である。
(1) 耐熱性ポリメラーゼ
PCR法で使用される耐熱性DNAポリメラーゼには、polI型、α型、混合型がある。
PCR法では、通常、family A(PolI型)に分類されているTaq DNAポリメラーゼおよびTth DNAポリメラーゼといった好熱性細菌Thermus aquaticus、Thermus thermophilus由来のDNAポリメラーゼが使用されている。比較的高温に耐えることができるが、90℃以上では半減期が大幅に短くなる。耐熱性が不十分なため、強い二次構造やGCリッチな配列を持つDNAを増幅する場合は、高温で長期間の処理が必要になる場合があり、長鎖テンプレートの増幅には、多くのまたは追加のインキュベーション時間が必要となり、これが問題となることがある。これらの酵素は、合成エラーを較正するための3’→5’エキソヌクレアーゼ(校正)活性を持っていないので、反応が停止したり、最終的に誤ったDNA配列が増幅されたりする可能性があるといった欠点がある。
一方、family B (α型)に分類されているPfu DNAポリメラーゼは、熱水環境で見つかった古細菌Pyrococcus furiosusから単離され、95℃でTaq DNAポリメラーゼの20倍の耐熱性を持っている。他の主な超耐熱性DNAポリメラーゼには、古細菌のThermcoccus kodakarensis KDDI株に由来およびPyroroccus属の一種から得られたKOD DNAポリメラーゼ、GBD DNAポリメラーゼなどがある。古細菌のDNAポリメラーゼは非常に耐熱性があるが、超耐熱性のPfu DNAポリメラーゼは、Taq DNAポリメラーゼよりも処理能力が低いため、DNA合成の伸長能力が低下するという欠点があり、また、これらの酵素は3’→5’エキソヌクレアーゼ(校正)活性を持っているため、PCRの正確性が高い。
(2) LA PCR用のポリメラーゼ
TaKaRa Exb Taq®、TaKaRa La Taq®は、3’→5’エキソヌクレアーゼ(校正)活性を含む耐熱性DNAポリメラーゼである。間違った塩基を取り込んだ場合、その後の反応性は非常に悪くなる。したがって、これを3’→5’エキソヌクレアーゼ活性で除去しスムーズに反応を進めることで、結果として長鎖DNAを増幅することができる。
(3) ホットスタート用のDNAポリメラーゼ
プライマーの融解温度(Tm)は50℃以上に設定されることがよくある。PCR反応液を調製してからサーマルサイクラーの温度が上昇するまで、室温〜50℃の温度範囲では弱いながらPCR反応液は活性を示すことから、ミスアニールしたプライマーを起点として反応が起こり、プライマータイマーやエキストラバンドなど非特異的増幅反応の原因となる。この反応を回避する方法として、ポリメラーゼの中和抗体を用いたホットスタート技術が開発され、中和抗体とポリメラーゼをあらかじめ混合することにより、室温〜60℃程度の温度範囲でポリメラーゼ活性を阻害することができる。この原理に基づくホットスタート用のDNAポリメラーゼが各試薬会社から提供されている。
5.2 RNA依存性DNAポリメラーゼ
これは逆転写酵素と呼ばれ、一本鎖RNAをテンプレートとして使用して5’→3’方向に相補DNAを合成するもので、次の2つのタイプがある。 1段階法によるRT-PCR法では逆転写活性を持つ耐熱性DNAポリメラーゼ(Tth DNAポリメラーゼなど)をcDNA酵素として使用し、2段階法ではcDNA合成とPCR法は、逆転写酵素と耐熱性DNAポリメラーゼをそれぞれ使用して実施される。モロニーマウス白血病ウイルス(MMLV)やトリ骨髄芽球症ウイルス(AMV)などのレトロウイルスに由来する逆転写酵素がcDNAシンターゼとして使用されている。
(1) 制限酵素
制限エンドヌクレアーゼとも呼ばれる制限酵素は、二本鎖DNAの特定の塩基配列を認識して切断する微生物由来の酵素である。制限酵素は、構造の複雑さ、認識配列の切断位置、および補因子の要件に従って分類されている。この酵素の名前は分離された細菌の学名に基づいており、遺伝子工学で広く使用されている。制限酵素は一般に4〜8塩基対(bp)の長さで、粘着末端(5’または3’突出末端)と呼ばれ、切断によって制限酵素断片を形成するものと、断片を残さない平滑末端を形成するものがあり、多くの塩基配列はパリンドローム(回分)構造を持っている。
(2) DNase I
DNase Iは、一本鎖および二本鎖DNAを分解して、5′-リン酸基を含むモノヌクレオチドまたはオリゴヌクレオチドを生成する反応を触媒する酵素である。
(3) RNase A
RNase Aはピリミジン残基の3’末端で一本鎖RNAを切断して、3’末端にピリミジン残基を持つオリゴリボヌクレオチド3’ホスホオキシドを生成するエンドリボヌクレアーゼである。
(4) DNAリガーゼ
一般的なDNAリガーゼは、ホスホジエステル結合を持つ二重らせんの隣接するDNA鎖の5′-P末端と3′-OH末端を結合する酵素である。補酵素としてATPが必要であり、反応の媒体として酵素-ATP複合体が形成される。これはDNAに作用し、突出端と平滑末端の両方を接続する。バクテリオファージT4に由来するT4 DNAリガーゼがよく使用されている。
5. Main enzymes used for testing
DNA synthase is a general term for enzymes that synthesize a DNA strand having a base sequence complementary to it using a single-stranded nucleic acid as a template. There are two types: DNA-dependent DNA polymerase that synthesizes DNA using DNA as a template, and RNA-dependent DNA polymerase that synthesizes DNA using RNA as a template.
Since there are various types of DNA synthases, it is necessary to understand the characteristics of each when performing a PCR test before selecting the enzyme required for the test.
5.1 DNA synthase (DNA polymerase)
Using DNA as a template, it is an enzyme that binds complementary dNTPs to the 3’end of the daughter strand and prolongs the strand. This enzyme reads the DNA parent strand in the 3’→ 5’direction and prolongs and synthesizes a new strand (daughter strand) complementary to the parent strand in the 5’→ 3’direction. The substrate of the polymerase is four kinds of deoxyribonucleoside triphosphates (dATP, dGTP, dCTP, dTTP). DNA-dependent DNA polymerase is an enzyme that plays a central role in DNA replication and DNA repair.
(1) Thermostable polymerase
The thermostable DNA polymerase used in the PCR method includes polI type, α type, and mixed type.
In the PCR method, DNA polymerases derived from Thermus aquaticus and Thermus thermophilus, which are thermophilic bacteria such as Taq DNA polymerase and Tth DNA polymerase, which are usually classified into family A (PolI type), are used. It can withstand relatively high temperatures, but its half-life is significantly shorter above 90℃. Due to insufficient heat resistance, high temperature and long-term treatment may be required when amplifying DNA having a strong secondary structure or GC-rich sequence. Amplifying long-chain templates can also require a lot of or additional incubation time, which can be problematic. These enzymes do not possess the 3’→ 5’exonuclease (proofreading) activity to calibrate synthetic errors, which may stop the reaction or eventually amplify the incorrect DNA sequence. It has the drawback of being there.
On the other hand, Pfu DNA polymerase, which is classified as family B (type α), is isolated from the archaea Pyrococcus furiosus found in hydrothermal environment and has 20 times higher heat resistance than Taq DNA polymerase at 95℃. Other major superheat-resistant DNA polymerases include KOD DNA polymerases and GBD DNA polymerases derived from the archaeal Thermococcus kodakarensis KDDI strain and derived from a species of the genus Pyroroccus. Archaeal DNA polymerases are extremely heat resistant, but they also have drawbacks. Since the super thermostable Pfu DNA polymerase has a lower processing capacity than the Taq DNA polymerase, it has a drawback that the elongation capacity of DNA synthesis is lowered. Moreover, since these enzymes possess 3’→ 5’exonuclease (proofreading) activity, the accuracy of PCR is high.
(2) Polymerase for LA PCR
TaKaRa Ex Taq®, TaKaRa La Taq® is a thermostable DNA polymerase containing 3’→ 5’exonuclease (proofreading) activity. If the wrong base is taken in, the subsequent reactivity will be extremely poor. Therefore, by removing this with 3’→ 5’exonuclease activity and proceeding with the reaction smoothly, long-chain DNA can be amplified as a result.
(3) DNA polymerase for hot start
The melting temperature (Tm) of the primer is often set to 50℃ or higher. From the time that the PCR reaction solution is prepared until the temperature of the thermal cycler rises, the PCR reaction solution shows activity while being weak in the temperature range of room temperature to 50℃. Therefore, the reaction starts from the misannealed primer. It occurs and causes non-specific amplification reactions such as primer timers and extra bands. As a method to avoid this reaction, a hot start technique using a neutralizing antibody of the polymerase has been developed, and by mixing the neutralizing antibody with the polymerase in advance, the polymerase activity is inhibited in a temperature range of about room temperature to 60℃. It is provided by each reagent company as a DNA polymerase for hot start.
5.2 RNA-dependent DNA polymerase
It is called reverse transcriptase and synthesizes complementary DNA in the 5’→ 3’direction using single-strand RNA as a template. In the 1-step method of the RT-PCR method, a heat-resistant DNA polymerase having reverse transcription activity (Tth DNA polymerase, etc.) is used as the cDNA enzyme, and in the 2-step method, the cDNA synthesis and the PCR method are performed with the reverse transcriptase and the heat-resistant DNA polymerase, respectively. Do it with two types. Reverse transcriptase derived from retroviruses such as Moloney murine leukemia virus (MMLV) and avian myeloblastosis virus (AMV) is used as the cDNA synthase.
(1) Restriction enzymes
The restriction enzyme, also called a restriction endonuclease, is a microorganism-derived enzyme that recognizes and cleaves a specific base sequence of double-stranded DNA. Restriction enzymes are broadly classified according to structural complexity, recognition sequence cleavage location, and cofactor requirements. The name is based on the scientific name of the isolated bacterium and is widely used in genetic engineering. Restriction enzymes are generally 4 to 8 base pairs (bp) long and are called sticky ends (5’or 3’protruding ends) that form restriction enzyme fragments by cleavage and blunt ends that do not leave fragments. Most of the base sequences have a palindromic structure.
(2) DNase I
DNase I is an enzyme that catalyzes the reaction that degrades single-stranded and double-stranded DNA to produce mononucleotides or oligonucleotides containing 5′-phosphate groups.
(3) RNase A
An endoribonuclease that cleaves single-stranded RNA at the 3’end of a pyrimidine residue to produce an oligoribonucleotide 3’phosphooxide with a pyrimidine residue at the 3’end.
(4) DNA ligase
A common DNA ligase is an enzyme that links the 5′-P and 3′-OH ends of adjacent DNA strands in a double helix with a phosphodiester bond. ATP is required as a coenzyme, and an enzyme-ATP complex is formed as a medium in the reaction. This acts on the DNA and can connect both protruding ends and blunt ends. T4 DNA ligase derived from Escherichia virus T4 is often used.
参考文献
(一社)日本臨床衛生検査技師協会(監修):遺伝子・染色体検査技術教本、丸善出版(2019)
(一社)日本臨床衛生検査技師協会(監修):微生物検査技術教本、丸善出版(2017)
(一社)日本遺伝子分析科学同学院(編集):遺伝子分析科学、宇宙堂矢次書店(2016)
(一社)環境DNA技術学会(企画)・土居秀幸・近藤倫生(編集):環境DNA、共立出版(2021)
掲載日:2022年1月20日
更新日:
References
Publication date: January 20, 2022
Updated:



