Nitrogen Cycle and Removal from Wastewater
村上定瞭(水浄化フォーラム), Sadaaki Murakami (Water & Solutions Forum)
1.窒素の循環
(1)生物による窒素の取込
(2)生物界での窒素循環
(3)生物による空中窒素の固定
(4)生物による脱窒素
(5)工業的窒素固定
2.窒素の化学と除去
(1)アンモニアの工業生産
(2)工業的な窒素除去
3.微生物によるアンモニア酸化(硝化)
4.微生物による脱窒素(脱窒)
(1)脱窒反応
(2)脱窒速度の影響因子
5.生物学的窒素除去プロセス-硝化脱窒法
(1)一相汚泥方式
(2)二相汚泥方式
(3)三相汚泥方式
6.生物学的窒素除去プロセス – アナモックス法
(1)アナモックス反応
(2)アナモックス菌叢と生理特性
(3)アナモックスリアクター
(4)アナモックス実施例
DOの意味とその制御
参考文献
関連ページ:リンの除去
1. Nitrogen cycle
(1) Biological nitrogen uptake
(2) Nitrogen cycle in biological world
(3) Biological nitrogen fixation from the air
(4) Biological denitrification
(5) Industrial nitrogen fixation
2. Chemistry and removal of nitrogen
(1) Industrial production of ammonia
(2) Industrial nitrogen removal
3. Ammonia oxidation (nitrification) by microorganisms
4. Denitrification by microorganisms
(1) Denitrification reaction
(2) Factors affecting denitrification rate
5. Biological nitrogen removal – nitrofication-denitrofication process
(1) One-phase sludge system
(2) Two-phase sludge system
(3) Three-phase sludge system
6. Biological Nitrogen Removal – Anammox process
(1) Anammox reaction
(2) Anammox flora and physiological characteristics
(3) Anammox reactors
(4) Anammox applictions
Meaning of DO and its control
References
Related page: Phosphorus removal
1.窒素の循環
(1)生物による窒素の取込
タンパク質や核酸などの有機窒素化合物に含まれる窒素は植物が土壌中(水域の低質を含む)から吸収した無機窒素化合物に由来する。植物(生産者)は、根を通して土壌中の硝酸イオン(NO3–)やアンモニウムイオン(NH4+)を吸収し、それを基にタンパク質や核酸などをつくる。生物が外界から無機窒素化合物を取り込み、自身のからだに必要な有機化合物をつくり変えるはたらきを窒素同化という。
1. Nitrogen cycle
(1) Biological nitrogen uptake
Nitrogen contained in organic nitrogen compounds such as proteins and nucleic acids is derived from inorganic nitrogen compounds uptaked by plants from soil (including low quality water bodies). Plants (producers) uptake nitrate ions (NO3–) or ammonium ions (NH4+) in the soil through the roots, and make proteins and nucleic acids based on the uptake. The function that organisms take up inorganic nitrogen compounds from the outside world and make organic compounds necessary for their bodies is called nitrogen assimilation.
(2)生物界での窒素循環
炭素の循環と同様に、植物が動物(消費者)に食べられると、窒素化合物は動物に移る。また、動植物の排泄物・枯死体の窒素化合物は、土壌中の菌類と細菌(分解者)に移り、アンモニウムイオンへと分解され、さらに硝化菌(亜硝酸菌・硝酸菌)によって硝酸イオンに変えられる。その後、再び植物に利用される。
(2) Nitrogen cycle in biological world
Similar to the carbon cycle , when plants are eaten by animals (consumers), nitrogen compounds are transferred to the animals. Nitrogen compounds in animals and plants excretions and dead bodies are transferred to fungi and bacteria (decomposers) in the soil, decomposed into ammonium ions, and then converted to nitrate ions by nitrifying bacteria (nitrite bacteria and nitrate bacteria ). After that, it is used again for plants.
(3)生物による空中窒素の固定
大気中には約80%もの窒素が含まれているが、窒素分子(N2)は安定な物質なので、多くの生物は直接これを利用できない。土壌菌中のアゾトノバクターやクロストリジム、マメ科植物の根に共生する根粒菌、ある種のシアノバクテリアなどは、空気中の窒素をアンモニアに変換する。これを窒素固定という。
(3) Biological nitrogen fixation from the air
The atmosphere contains about 80% nitrogen, but nitrogen molecule (N2) is stable and cannot be directly used by many organisms. Azotonobacter and Clostridim in soil prokaryotes, root nodule bacteria symbiotic with the roots of legumes, and certain cyanobacteria convert nitrogen molecule in the air into ammonia. This is called biological nitrogen fixation.
(4)生物による脱窒素
水中や土壌中には、亜硝酸・硝酸イオンを窒素分子に変えて大気中に放出する脱窒素細菌(脱窒菌)が存在し、この反応を脱窒という。
(4) Biological denitrification
Denitrifying bacteria, that convert nitrite and nitrate ions into nitrogen molecules and release them into the atmosphere are present in water and soil, and these reactions are called denitrification.
(5)工業的窒素固定
大気中の窒素と水素を化合し、アンモニアを工業的に生産(工業固定)し、肥料・合成繊維などの原料としている。特に、化学肥料を使用して食料・飼料を生産しているため、生物界を循環する窒素の総量が大幅に増加している。
目次へ
(5) Industrial nitrogen fixation
By combining gaseous nitrogen and hydrogen and producing ammonia industrially (fixed industrially), it is used as a raw material for fertilizers and synthetic fibers. In particular, since chemical fertilizers are used to produce food and feed, the total amount of nitrogen circulating in the living world has increased significantly.
To table of contents
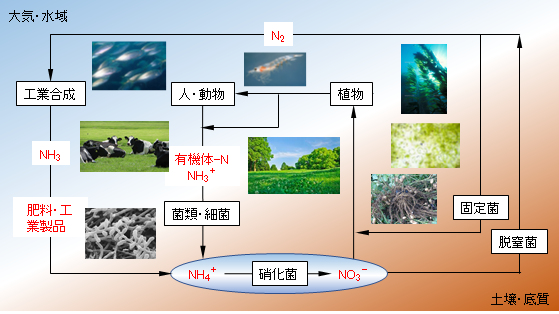
図1 窒素の循環 Fig.1 Nitrogen circulation.
2.窒素の化学と除去
(1)アンモニアの工業生産
窒素と水素を原料として、400~500℃、200~350気圧において四酸化鉄Fe3O4を主成分とする触媒を用いて合成する(ハーバー・ボッシュ法)。このアンモニアは主に肥料・化学繊維(ナイロン)の原料や排煙脱硝などに用いられる。
2. Chemistry and removal of nitrogen
(1) Industrial production of ammonia
Ammonia is synthesized from nitrogen and hydrogen as raw materials at 400 to 500°C and 200 to 350 atm using a catalyst containing iron tetroxide Fe3O4 as the main component (Haber-Bosch method). This ammonia is mainly used as a raw material for fertilizers and chemical fibers (nylon) and flue gas denitration.
(2)工業的な窒素除去
気体状窒素化合物
石炭利用の火力発電所などから排出される窒素酸化物(NOx)や内燃機関での酸素と窒素の結合による生成するNOxの除去には、アンモニア・尿素・シアン化水素などの窒素化合物や炭化水素・水素などの化合物を用いてNOxを窒素ガスへ変換する方法が用いられる。高温・高圧下で反応が進行するが、触媒を用いて反応条件を緩和する。
火力発電所に広く用いられている排煙脱硝法では、排ガス中にアンモニアを注入し、二酸化チタンを主成分としバナジウム、タングステンなどが添加された触媒上でNOxを選択的に反応させて窒素と水に変換する。
(2) Industrial nitrogen removal
Gaseous nitrogen compounds
Nitrogen oxides (NOx) are emitted from such as coal-fired thermal power plants and NOx produced by the combination of oxygen and nitrogen in internal combustion engines. NOx are removed by a method of converting NOx to nitrogen gas using nitrogen compounds such as ammonia, urea, hydrogen cyanide, hydrocarbons and hydrogen. Although the reaction proceeds at high temperature and high pressure, the reaction conditions are relaxed using a catalyst.
In the flue gas denitration method widely used in thermal power plants, ammonia is injected into the exhaust gas, NOx is selectively reacted on a catalyst containing titanium dioxide as a main component and vanadium, tungsten, etc., to react with nitrogen, and converted to nirogen N2 and water.
液体中窒素化合物
硝酸・亜硝酸イオンとアンモニウムイオンを等モル含む水溶液を超臨界・亜臨界の高温・高圧の状態にすると不均化反応により分子状窒素と水分子が生成する。遷移金属(特に、筆者らの実験ではモリブデン・ロジウムの効果が高い)を触媒として用いると、300℃以下の温度でも95%以上の脱硝効果が得られる。この方法は、装置が複雑で高価であるので、極めて高濃度の窒素廃液処理(数千~数万mgN/L)に限定される。
目次へ
Nitrogen compounds in liquid
When an aqueous solution containing equimolar amounts of nitric acid/nitrite ion and ammonium ion is brought to a supercritical/subcritical state at high temperature and high pressure, molecular nitrogen and water molecule are generated by the disproportionation reaction. When a transition metal (especially in our experiments, the effect of molybdenum and rhodium is highly effective) is used as a catalyst, a denitration effect of 95% or more can be obtained even at a temperature of 300°C or less. This method is limited to an extremely high-concentration nitrogen waste liquid treatment (thousands to tens of thousands mg-N/L) because the system is complicated and expensive.
To table of contents
3.微生物によるアンモニア酸化(硝化)
アンモニアの硝酸イオンへの微生物による酸化は2段階で行われる。酸素存在下で、ニトロソモナス属・ニトロソコッカス属など(亜硝酸菌)によって亜硝酸イオンに変換される。亜硝酸イオンは、ニトロソバクター属など(硝酸菌)によって硝酸イオンに変換される。
これらの反応(上記双方の細菌群を硝化菌)によって、酸素ががモル比(O/N)で3.5倍量、重量比で4.57倍量消費される。また、水素イオンがモル比(H/N)で2倍量生成するので、水酸化ナトリウム(NaOH)換算で5.72gのアルカリが必要となる。それぞれの硝酸菌の最大増殖速度のpH(亜硝酸菌、pH6.5付近;硝酸菌、pH8.5付近)が異なりpH設定値によって律速段階が異なるので、これらの反応の制御は可能であるが、簡単ではない。
3. Ammonia oxidation (nitrification) by microorganisms
The microbial oxidation of ammonia to nitrate is carried out in two steps. In the presence of oxygen, (1) it is converted to nitrite by nitrite bacteria such as Nitrosomonas and Nitrosococcus, (2) nitrite ion is converted into nitrate ion by Nitrosobacter.
Oxygen is consumed 3.5 times in molar ratio (O/N) and 4.57 times in weight ratio by these reactions (nitrifying bacteria of both bacteria groups). In addition, since hydrogen ions are produced in a double amount in molar ratio (H/N), 5.72 g of alkali is required in terms of sodium hydroxide (NaOH). It is possible to control these reactions because the pH of the maximum growth rate of each nitric acid bacterium (nitrite bacteria, around pH 6.5; nitric acid bacteria, around pH 8.5) is different and the rate-determining step differs depending on the pH setting value, but it is not easy.
水温
硝化細菌は10~35℃で生育可能であるが、適温は20~30℃で、15℃では25℃の1/2に反応速度が低下する。窒素除去型浄化槽では、水温13℃以上で適正に硝化・脱窒素反応が進行するように、装置の構造基準が定められている。
Temperature
Nitrifying bacteria can grow at 10 to 35°C, but the optimum temperature is 20 to 30°C, and the reaction rate decreases to 1/2 of 25°C at 15°C. In the nitrogen removal type septic tank, the structural standard of the equipment is set so that the nitrification and denitrification reaction proceed properly at a water temperature of 13°C or higher.
pH
硝化菌の最適pHは6.5~8.5である。pHが低下すると硝化反応が進行しないので、アルカリ度が不足する汚水処理では、アルカリ添加によるpH制御が必要となる。
pH
The optimum pH of nitrifying bacteria is 6.5 to 8.5. When the pH is lowered, the nitrification reaction does not proceed, so in sewage treatment where the alkalinity is insufficient, pH control by the addition of alkali is necessary.
有機物濃度
有機物がBOD換算でおよそ30mg/L以上存在すると、硝化反応は進行しないので、曝気時間を十分とって有機物を低濃度に維持することが必要である。
Organic matter concentration
When the organic matter is present in an amount of about 30 mg/L or more in terms of BOD , the nitrification reaction does not proceed, so it is necessary to maintain a low concentration of the organic matter by taking sufficient aeration time.
DO
数mg/Lに設定する。特にその数値に拘る必要はない。1mg/L以下では、DO計の検定が不適切である場合やDO測定への妨害物質(酸素センサーの隔膜を通過する分子状電子供与体)が共存する場合には、DOが本当に酸素供給量が適正状態であるかどうか判定ができない。
DO
Set to a few mg/L. If the DO is less than 1 mg/L, it is not possible to judge whether the oxygen supply is really appropriate, when the calibration of the DO meter is inappropriate or when an interfering substance (for example, a molecular electron donor passing through the membrane of the electrochemical oxygen sensor) coexists for DO measurement.
汚泥令
一般的な有機物酸化菌の増殖速度は3.0~13.2/日に対して、硝化菌は0.34~13.2/日と一桁低い値である。汚泥令(SRT、汚泥滞留日数)は6~10日が最適といわれるが、7日以上確保する。
なお、生物学的窒素除去法では、システムを開始して、正常に稼働するまでに数週間が必要となる。まず、有機物酸化菌が増殖し有機性窒素が分解されてアンモニアが生成し、次にアンモニアを亜硝酸イオン、硝酸イオンへそれぞれ酸化する細菌が逐次増殖して、それぞれの機能が発揮されるからである。参考までに、魚の飼育水槽(水温15℃)を浸漬ろ床法で浄化するシステム(閉鎖系)でのアンモニア・亜硝酸・硝酸性窒素の濃度変化を別ページに示しているので、参考にされたい。
目次へ
Sludge retention time
The growth rate of general organic matter oxidizing bacteria is 3.0 to 13.2/day, whereas that of nitrifying bacteria is 0.34 to 13.2/day, which is an order of magnitude lower. It is said that the optimal sludge age (SRT, sludge retention days) is 6 to 10 days, but secure at least 7 days.
It should be noted that the biological nitrogen removal method requires several weeks after the system is started to operate normally. First, organic matter-oxidizing bacteria proliferate and organic nitrogen is decomposed to produce ammonia, and then bacteria that oxidize ammonia to nitrite ion and nitrate ion respectively proliferate sequentially and exert their respective functions. For reference, another page shows the changes in the concentrations of ammonia, nitrite, and nitrate nitrogen in a system (closed system) for purifying a fish tank (water temperature: 15°C) by the immersion filter method.
To table of contents
4.微生物による脱窒素(脱窒)
(1)脱窒反応
脱窒菌
脱窒菌は、土壌中や水域の底泥表層中に広く存在する。有機物(水素源)を必要とする従属栄養性の通性嫌気性菌であり、酸素が存在する場合にはこれを利用して呼吸するが、無酸素状態では硝酸・亜硝酸イオンなどの結合酸素を呼吸反応に利用する。脱窒反応は硝酸呼吸とも呼ばれる。
4. Denitrification by microorganisms
(1) Denitrification reaction
Denitrifying bacteria
Denitrifying bacteria are widely present in soil and surface layer of bottom mud in water bodies. These are heterotrophic facultative anaerobic bacteria which requires organic matter (hydrogen source). These utilize oxygen to breathe when it is present, but do chemical bounding oxygen such as nitrate and nitrite ions for respiratory reactions in the anaerobic state. These denitrification reactions are also called nitrate respiration.
有機物量
脱窒反応には、BOD必要量は、亜硝酸イオンで窒素に対して1.7倍量、硝酸イオンで2.9倍量が消費される。メタノール必要量は、亜硝酸イオンで窒素に対して1.1倍量、硝酸イオンで1.9倍量が消費される。
メタノール添加では、汚水中窒素に対して、余裕を見て1.5倍量、2.5倍量をそれぞれ添加するとよい。なお、メタノール添加・脱窒工程の後、放流する場合には、沈殿槽の前に残存するメタノールを除去するための再曝気槽の設置が必要となる。
Organic matter amount
In the denitrification reaction, the required amount of BOD is 1.7 times as much as nitrogen for nitrite ion or 2.9 times as much as for nitrogen for nitrate ion. Nitrite ion consumes methanol 1.1 times the amount of nitrogen, or nitrate ion consumes it 1.9 times.
When adding methanol, it is advisable to be added 1.5 times or 2.5 times the amount of nitrogen to wastewater with a margin. In addition, in the case of discharging treated water after denitrification process, it is necessary to install a re-aeration tank for removing the residual methanol before the precipitation tank.
(2)脱窒速度の影響因子
水温
脱窒菌の活性に与える水温の影響は、通常の有機物分解菌と同等であり、一般的な脱窒速度は、20℃において、水素供与体として有機物を使用した場合0.1kg-N/kg-VSS/日程度、メタノールを使用した場合0.2kg-N/kg-VSS/日程度の値を適用する。
(2) Factors influencing denitrification rate
Temperature
The effect of water temperature on the activity of denitrifying bacteria is equivalent to that of ordinary organic substance degrading bacteria, and the general denitrifying rate is about 0.1 kg-N/kg-VSS/day at 20°C when organic substances are used as hydrogen donors. If methanol is used, apply a value of 0.2 kg-N/kg-VSS/day.
pH
脱窒反応の最適pHは7~8であり、中性であればよい。
脱窒反応ではOH–が生成するので、pHが上昇する。硝酸・亜硝酸イオン濃度が高い汚水を処理する場合には、塩酸・硫酸等によりpH調整が必要となる。
pH
The optimum pH for the denitrification reaction is 7 to 8 and may be neutral. In the denitrification reaction, OH– is produced and the pH rises. When treating sewage having a high nitric acid/nitrite ion concentration, it is necessary to adjust the pH with hydrochloric acid, sulfuric acid, or the like.
汚泥発生量
硝化工程では流入窒素の約5%が菌体となる。脱窒工程では、メタノールの添加量を2.5倍量とすると、その約20%が菌体となる。したがって、汚水中の窒素の50%の汚泥が発生することとなる。
Amount of sludge generated
In the nitrification process, about 5% of the inflowing nitrogen becomes bacterial cells. In the denitrification process, if the amount of methanol added is 2.5 times the amount, about 20% will be bacterial cells. Therefore, 50% of the nitrogen in the sewage will be sludge.
リンの必要量
菌体中のリン含有量は1~2%であるので、窒素量に対し0.5~1%のリンが必要となる。生活系排水ではリンの添加は不要であるが、工場排水ではリンが存在しないことが多く、適宜、リンを添加することが必要となる。
目次へ
Required amount of phosphorus
Since the phosphorus content in the bacterial cells is 1 to 2%, 0.5 to 1% of phosphorus is required for the nitrogen content. It is not necessary to add phosphorus to domestic wastewater, but phosphorus is often absent in factory wastewater, and it is necessary to add phosphorus as appropriate.
To table of contents
5.生物学的窒素除去 – 硝化脱窒法
生物学的脱窒においては、硝化反応と脱窒反応を合理的に行わせ、先に述べた硝化菌・脱窒菌の生理特性を考慮した上で処理プロセスを構成する。
硝化菌・脱窒菌を汚水処理に適用する基本的な要素は、①微生物群の保持方法、②好気槽・無酸素槽などの槽配列とその流動形態である。微生物の保持形態(培養法)としては浮遊型(活性汚泥法)か付着型(生物膜法)か、反応槽の形状・規模、汚水滞留時間・流動形式などである。一般的に小・中型処理装置には生物膜法、大型処理装置では活性汚泥法がそれぞれ用いられる。各反応槽の配置・流動形式で分類すると、間欠曝気型と連続曝気型に区分できる。
生物型窒素除去法は有機物酸化・硝化・脱窒を行わせるための反応槽と沈殿池の組合せによっていくつかの方式に分けられる。硝化槽ではアルカリ度が減少し、脱窒槽では増加するとともに有機物が必要である。曝気槽で有機物の酸化分解と硝化を同時に進め、その後で脱窒反応を行う方法(図2(A)や図3(D))では有機物やアルカリ度の活用からみて効果的ではない。無酸素槽を前置して、硝化液を循環する方式が多用される(図2(B))。この方式には、脱窒工程を硝化工程の前後に配置させる方式または脱窒槽・硝化槽の順に組合せ硝化液を循環させる方式がある。水素源として流入水中の有機物を、また硝化のためのアルカリ分を脱窒液に求める方式が多い。生活排水などへは、汚水中の有機成分を有効に利用することができ、しかも硝化脱窒時のpH変動を低く抑えることができる硝化液循環型の処理プロセス(図2(B))が広く用いられている。
以上述べた生物学的窒素除去法は有機物酸化・硝化・脱窒をおこなわせるための反応槽と沈殿池の組合せによって図2及び図3に示すように分けられる。
5. Biological Nitrogen Removal – Nitrification-Denitrification Process
In biological denitrificatin, the reactions of nitrification and denitrification are rationally performed, and the treatment process is configured in consideration of the physiological characteristics of both nitrifying and denitrifying bacteria described above.
The basic elements that apply nitrifying and denitrifying bacteria to wastewater treatment are (1) the method for holding the microorganism group, (2) the arrangement of tanks such as aerobic and anaerobic tanks, and their flow forms. The microbial retention form (culturing method) may be a floating type (activated sludge method) or an attachment type (biofilm method), the shape and scale of the reaction tank, the wastewater retention time, and the flow type. In general, the biofilm method is used for small/medium-sized treatment system, and the activated sludge method is used for large treatment system. When classified according to the arrangement and flow type of each reaction tank, it can be classified into an intermittent aeration type and a continuous aeration type.
The biological nitrogen removal method can be divided into several methods depending on the combination of a reaction tank and a sedimentation tank for performing organic substance oxidation, nitrification, and denitrification. In the nitrification tank, the alkalinity decreases, and in the denitrification tank, the alkalinity increases and organic matter is required. The method of simultaneously promoting oxidative decomposition and nitrification of organic substances in the aeration tank and then performing the denitrification reaction (Fig.2(A) and Fig.3(D) ) is not effective from the viewpoint of utilizing organic substances and alkalinity. A system, in which an anaerobic tank is placed in front and the nitrification solution is circulated, is often used (Fig.2(B)). This method includes a method of arranging the denitrification step before and after the nitrification step, or a method of circulating a combined nitrification solution in the order of the denitrification tank and the nitrification tank. There are many methods in which organic matter in the inflow wastewater is used as a hydrogen source and an alkali content for nitrification is obtained in the denitrification liquid. A wide range of nitrificated solution circulation type treatment processes (Fig.2(B)) that can effectively use organic components in wastewater for domestic wastewater treatment and can keep pH-fluctuations low during nitrification and denitrification reactions.
The biological nitrogen removal method described above can be divided as shown in Figs.2 to 3 depending on the combination of the reaction and sedimentation tanks for performing the oxidation of organic matter, nitrification and denitrification.
(1)一相汚泥方式
単一の活性汚泥中に有機物酸化菌・硝化菌・脱窒菌を共存培養する方式で複数の反応槽(活性汚泥でも生物膜でもより)と1つの沈殿池を最終的に設ける。プロセスの構成は簡単になるが、それぞれの細菌群の間で拮抗作用が起こる可能性がある。1槽を曝気槽とし、他の1槽を無酸素状態(微生物と汚水を接触させる攪拌が必要)で汚泥を保持して各微生物群を活用する方式である。最も所有面積が少なくてすむが、汚泥管理を十分にする必要がある。
図2(A)は、第1槽で有機物・アンモニアを同時に参加して、残存する亜硝酸・硝酸イオンを攪拌(無酸素)槽で水素供与体(有機物)を添加して窒素ガスに変換する方式である。なお、水素供与体を添加する方式では、脱窒素(無酸素)槽の後段に再曝気槽を設置するが、図中では省略してある。これは脱窒槽で供給された水素供与体(メタノールなど)の残存分の除去を目的とする。以下、同様である。
同(B)は、第2槽(曝気槽)の亜硝酸・硝酸イオン含む硝化液を第1槽(無酸素槽)へ循環して、流入水の有機物を水素源として脱窒反応を行う。生活排水系では、循環量は流入水の3~4倍が最適といわれている。この方式では、汚水中の有機成分を有効に利用することができ、しかも硝化脱窒時のpH変動を低く抑えることができる。流入汚水中の有機物(BOD)/Nの割合がおよそ3倍以上であれば、水素供与体の添加は不要である。
同(C)(間欠ばっ気法)は、上記(B)(連続曝気法)の変法で、曝気(有機物酸化・硝化)および攪拌(無酸素)を一定間隔で繰り返して、硝化・脱窒反応を交互に行うシステムである。
攪拌には機械攪拌、ポンプ攪拌、ガス攪拌などがあるが、ガス攪拌の場合には曝気装置の兼用が可能である。
(1) One-phase sludge method
A plurality of reaction tanks (available both to activated sludge and biofilm systems) and one settling basin are finally installed by the method of co-culturing organic matter oxidizing bacteria, nitrifying bacteria, and denitrifying bacteria in a single activated sludge . Although the process is simple to configure, antagonism may occur between each bacterial group. This is a system in which one tank is used as an aeration tank and the other tank is used as an oxygen-free(anaerobic) state (needs to stir to bring microorganisms and wastewater into contact with each other) to hold sludge and utilize each microorganism group. It has the smallest owned area, but sufficient sludge management is required.
In Fig. 2(A) , it is a method that organic substances and ammonia are simultaneously participated in the first tank, and the remaining nitrite and nitrate ions are converted into nitrogen gas by consuming a hydrogen donor (organic substances) in a stirring (anaerobic) tank. In this system, a re-aeration tank with adding a hydrogen donor is installed after the denitrification (oxygen-free) tank, but it is omitted in the figure. This is intended to remove the residual hydrogen donor (such as methanol) supplied in the denitrification tank. The same applies hereinafter.
In (B), the nitrification solution containing nitrite/nitrate ions in the second tank (aeration tank) is circulated to the first tank (oxygen-free tank) to carry out a denitrification reaction by using the organic matter in the inflow water as a hydrogen source. For the domestic wastewater system, it is said that the optimal circulation volume is 3 to 4 times that of the inflow water. With this method, the organic components in the wastewater can be effectively used, and the pH fluctuation during nitrification and denitrification can be suppressed to a low level. The ratio of organic matter (BOD)/N in the inflowing wastewater is about 3 times or more, if so, the addition of a hydrogen donor is unnecessary.
The (C) (intermittent aeration method) is a modified method of the above (B) (continuous aeration method), in which aeration (organic substance oxidation and nitrification) and stirring (oxygen-free) are repeated at regular intervals to perform nitrification and denitrification. It is a system in which reactions are alternately performed.
Mechanical, pump and gas agitations, and the like can be used for agitation, and in the case of gas agitation, the aeration device can also be used.
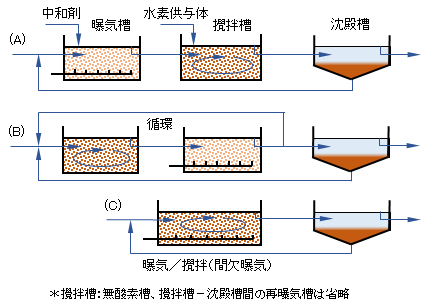
図2 一相汚泥式硝化脱窒プロセス
Fig.2 Nitrification and denitrification process by single-phase sludge.

写真1 一相汚泥・硝化液循環型窒素除去法の室内実験装置
装置(撹拌槽-3L、曝気槽-10L、沈殿槽-3L)、医・農薬製造排水-10L/日
Photo Indoor laboratory equipment for nitrogen removal method with circulations of one-phase sludge and nitrifyed solution.
Stirring tank: 3L, aeration tank: 10L, sedimentation tank: 3L, medical or agrochemical manufacturing wastewater: 10L/day.
(2)二相汚泥方式
図3(D)のシステムは、酸化と硝化を同一の反応相で行い、脱窒を別の反応槽で行う方式である。反応槽と沈殿槽はそれぞれ2つ必要となる。二相汚泥システムでは有機物酸化と硝化を第1槽で完了させ、脱窒を第2槽で実施する。曝気槽でのアルカリ添加と水素供与体としてメタノールなどの添加が必要となる。
(2) Two-phase sludge system
The system of Fig.3(D) is a system in which oxidation and nitrification are performed in the same reaction phase, and denitrification is performed in another reaction tank. Two reaction tanks and two settling tanks are required. In the two-phase sludge system, organic matter oxidation and nitrification are completed in the first tank, and denitrification is performed in the second tank. It is necessary to add alkali in the aeration tank and methanol as a hydrogen donor.
(3)三相汚泥方式
有機物の酸化・硝化・脱窒をすべて別々の微生物群汚泥を保持する反応槽を使って行う方式である。三相汚泥システムは、第1槽でBOD成分を代謝分解し、第2槽でアンモニウムイオンを硝化し、第3槽で無酸素状態で有機物を添加して亜硝酸・硝酸イオンを窒素ガスに変換する方式である。第2槽では硝化反応によりアルカリ度が消費され、pHが低下するため、そのアルカリ剤を添加してpH調整を行う。第3槽では所定量の有機物を添加する。本システムでは各微生物群を個別に培養するので、それぞれの微生物群の至適条件で維持管理できるので安定した処理が期待できる。しかし、汚泥の培養数に事例して沈殿槽が多くなる上にアルカリや有機物の添加が必要となり、建設費や維持管理費が高くなる。
汚水中に硝化菌あるいは脱窒菌に阻害効果のある物質が含まれている場合には、BOD酸化を主体とする活性汚泥プロセスを独立さて阻害物質を分解し、後段で二相汚泥または三相汚泥方式で窒素除去を行う。
目次
(3) Three-phase sludge system
This is a method in which the oxidation, nitrification, and denitrification of organic substances are all carried out using a reaction tank that holds separate microbial group sludge. The three-phase sludge system metabolizes and decomposes BOD components in the first tank, nitrifies ammonium ions in the second tank, and adds organic matter in the third tank in anaeroic state to convert nitrite and nitrate ions into nitrogen gas. In the second tank, the alkalinity is consumed by the nitrification reaction and the pH drops, so the pH is adjusted by adding the alkaline agent. A predetermined amount of organic matter is added to the third tank. Since this system cultures each microbial group individually, stable treatment can be expected because each microbial group can be maintained and managed under optimal conditions. However, as the number of sludge cultures increases, the number of settling tanks increases, and addition of alkalis and organic substances is required, resulting in high construction costs and maintenance costs.
When the wastewater contains substances that have an inhibitory effect on nitrifying bacteria or denitrifying bacteria, the active sludge process mainly composed of BOD oxidation is independently decomposed to decompose the inhibitors, and the two-phase sludge or three-phase sludge is used in the latter stage. Method to remove nitrogen.
To table of contents
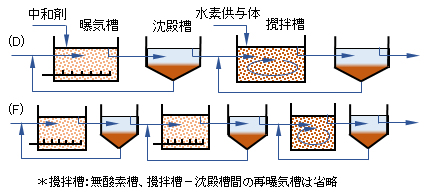
図3 二相汚泥式(D)・三相汚泥式(E)の硝化脱窒プロセス
Fig.3 Nitrification denitrification processses for two-phase sludge system (D) and three-phase sludge system (E).
6.生物学的窒素除去 – アナモックス法
6.1 アナモックス反応
(1) AMX反応とは
アナモックスとは嫌気性アンモニア酸化(anaerobic ammmonium oxidation、以下、AMXで略記する)の略称である。AMX反応は、図4(4)に示すように、NO2–を電子受容体とし、NH4+を嫌気的に酸化してN2へ変換する反応であり、オランダの下水処理場で初めて見出され1995年に報告された。NH4+をNO3–へ酸化した後、有機物を電子受容体としてNO3–をN2へ変換する硝化脱窒法と比べて、AMX法は使用電力および余剰汚泥の低減が可能となる技術である。
なお、微生物によるNH4+とNO2–との反応によるN2への変換については、1977年に予測されていた。また、NH4+を還元してN2へ変換する細菌・アーキアは、海洋・湖沼・土壌中などに幅広く存在し、好気的条件下でも前記反応を行う細菌の存在も確認されている(ただし、酸素を遮断する仕組みがあり、菌体内での反応は嫌気反応である。)。詳しくは、別ページで解説する。
6. Biological Nitrogen Removal – Anammox Process
6.1 Anammox Reaction
(1) What is Anammox reaction?
Anammox is an abbreviation for anaerobic ammmonium oxidation (hereinafter abbreviated as AMX). As shown in Fig.4, the AMX reaction is a reaction that uses NO2– as an electron acceptor and anaerobically oxidizes NH4+ to N2. It was first discovered at a sewage treatment plant in the Netherlands in 1995. Compared to the nitrification-denitrification method, which oxidizes NH4+ to NO3– and then converts NO3– to N2 using an organic substance as an electron acceptor, the AMX method is a technology that can reduce power consumption and excess sludge.
The conversion to N2 with the reaction of NH4+ and NO2– by microorganisms was predicted in 1977. In addition, bacteria and archaea that reduce NH4+ to N2 are widely present in the ocean, lakes, and soil, and the presence of bacteria, that perform the above reaction even under aerobic conditions, has been confirmed. There are mechanisms to block oxygen, and the reactions inside the bacteria are anaerobic reactions. Details will be explained on another page.
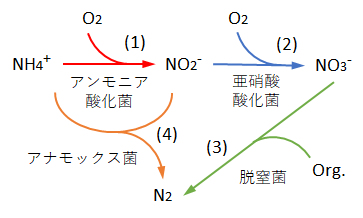
図4 アンモニアの生物学的酸化還元反応とそれらの酸化還元菌
Fig.4 Biological redox reactions of ammonia and their redox bacteria.
(2) AMX菌の増殖と制御
AMX反応は、一般的に次式で示され、1モルのアンモニアと1.3モルの亜硝酸を消費し、1 モルの窒素ガスと約0.3 モルの硝酸を生産する。
(2) Growth and control of AMX bacteria
The AMX reaction is generally represented by the following formula, which consumes 1 mol of ammonia and 1.3 mol of nitrite, and produces 1 mol of nitrogen gas and about 0.3 mol of nitric acid.
そこで、バイオリアクター内にAMX菌を保持するためには、次に示す方法などが必要となる。(a) 共存する阻害基質(有機物やNO3–など)を前もって除去し、酸素の存在下で、NH4+を半分量NO2–へ酸化する。(b) AMX菌のSRTを十分に長く保持するリアクターを工夫する。他の細菌類が共存する系では、(c) AMX菌をリアクター内に保持して系外へ流出しない方法か、あるいは (d) AMX菌のみを分離してリアクターへ返送する。
プロセス(a):有機物を除去した後、NO3–が生成しない条件で、NH4+の半分量を少し上回る程度に酸化してNO2–を生成させる(部分酸化)。
プロセス(b):AMX菌グラニュール法またはAMX菌を固定保持する担体法を用いる。
プロセス(c):好気・嫌気の両条件を満たし、AMX菌および他菌類を共存固定する担体へ保持する。
プロセス(d):他細菌とAMX菌との異なる性状を利用して汚泥を分離する。
AMX菌を利用した窒素除去法には、上記のいずれかのプロセスを組み合わせた工程が実用化されている。
Process (a): After removing organic matter, under the condition that NO3– is not produced, it is oxidized to a little more than half the amount of NH4+ to produce NO2– (partial oxidation).
Process (b): AMX bacteria granule method or carrier method for retaining AMX bacteria is used.
Process (c): Both aerobic and anaerobic conditions are satisfied, and AMX bacteria and other bacteria are retained on a carrier for coexistence and fixation.
Process (d): AMX bacterial sludge is isolated using the different properties of other bacterial sludges.
In the nitrogen removal method using AMX bacteria, a process combining any of the above processes has been put into practical use.
(3) AMX菌への影響因子
a) pHと温度
pH7~8.5、水温は30~37℃が最適であるとされる。脱窒の条件は、pH 6.9~7.9、水温は30~40℃であるので、最適条件は非常に似かよっている。低温域(12~15℃)で最大のAMX菌もいるが、処理速度の視点から、特殊な廃水処理に限られる。
b) NO2–、NH4+の阻害
NO2–は比較的低い濃度から阻害を示し、100mg/Lから阻害を示すと言われる。NH4+は、1,000mg/L前後以上で阻害を示すと言われる。遊離のNH3は数10~200mg/Lで阻害を示すとの報告がある。NH4+ ⇄ NH3 + H+ には平衡関係があり、pHの増加とともに、右方向へ平衡が移動するので、注意を要する。
c) 有機物の影響
有機物の影響は、その物質により大きく異なる。メタノールは数mg/Lのレベルで否可逆的な阻害を受ける。一方で、AMX菌は多様な代謝を示し、酢酸などを利用し、グルコース・ギ酸などには影響を受けない。しかしながら、有機物の存在は他の細菌類の増殖を促進するので、増殖率の遅いAMX菌の占有率が低下し汚泥管理による流出が問題となる。
d) 他の阻害因子
硫化物やリン酸は、それぞれ1や20mmol/Lレベルで阻害するとの報告がある。カチオン系ポリマーは1,000mg/Lレベルで阻害があるとされる。
(3) Factors affecting AMX bacteria
a) pH and temperature
The optimum pH is 7 to 8.5 and the water temperature is 30 to 37 ° C. The denitrification conditions are pH 6.9 to 7.9 and the water temperature is 30 to 40 ° C, so the optimal conditions are very similar. Some AMX bacterial growths are the largest in the low temperature range (12 to 15 ° C), but from the viewpoint of efficiency, they are limited to special wastewater treatment.
b) NO2–, NH4+ inhibition
NO2– is said to show inhibition from relatively low concentrations and inhibition from 100 mg/L. NH4+ is said to show inhibition at around 1,000 mg/L or higher. It has been reported that free NH3 inhibits at several tens to 200 mg/L. Note that NH4+ ⇄ NH3 + H+ has an equilibrium relationship, and the equilibrium shifts to the right as the pH increases.
c) Effects of organic matter
The effects of organic matter vary greatly depending on the substance. Methanol is irreversibly inhibited at levels of a few mg/L. On the other hand, AMX bacteria show various metabolisms, use acetic acid, etc., and are not affected by glucose, formic acid, etc. However, since the presence of organic matter promotes the growths of other bacteria, the occupancy rate of the slow-growing AMX bacteria decreases, and the outflow due to sludge management becomes a problem.
d) Other inhibitors
It has been reported that sulfide and phosphoric acid inhibit at 1 and 20 mmol/L levels, respectively. Cationic polymers are said to be inhibitory at 1,000 mg/L levels.
6.2 AMX菌叢および生理特性
AMX菌は、その濃度が高くなると赤く見える。これは、鉄タンパク質であるヒドラジン酸化酵素のためと考えられる。AMX菌は、海洋・河川・湖沼の底泥や汚水処理汚泥など、自然界の様々な場所で広くその存在が示されている。
AMXの純粋培養株は得られていないものの、分類上はBacteriaのPlanctomycetes門、Planctomycetia網、Candidatus Brocadiles目、Ca. Brocadiaceae科に属し、現在、Ca. Brocadia、Ca. Kuenenia、Ca. Jettenia、Ca. Anammoxoglobus、Ca. Scalindua、Ca. Anammoximicrobiumの6つの属提案されている。Ca.は、培養に成功していない生物につけられるCandidatusの略省である。
汚水処理で検出される多くは、Ca. BrocadiaとCa. Kueneniaである。詳しいAMX菌叢および生理学的特性については、Web等から検索・参考にされたい(例えば:https://www.eng.hokudai.ac.jp/labo/water/research_Annammox.html)。
6.2 AMX flora and physiological characteristics
AMX bacteria appear red at higher concentrations. This is thought to be due to the iron protein hydrazine oxidase. AMX bacteria have been widely shown to exist in various places in the natural world, such as the bottom mud of oceans, rivers and lakes, and sewage treatment sludge.
Although any pure culture strain of AMX bacteria has not been obtained, they belongs to family Ca. Brocadiacease, order Candidatus Brocadiles, class Planctomycetia, phylum Planctomycetes. Six genuses, Ca. Brocadia, Ca. Kuenenia, Ca. Jettenia, Ca. Anammoxoglobus, Ca. Scalindua, and Ca. Anammoximicrobium, have been proposed. Ca. is an abbreviation for Candidatus, which is attached to organisms that have not been successfully cultivated.
Most of the sewage treatments detected are Ca. Brocadia and Ca. Kuenenia. For detailed AMX flora and physiological characteristics, search and refer to them on the Web (for example: https://www.eng.hokudai.ac.jp/labo/water/research_Annammox.html).

写真2 担体に固定されたAMX菌 Photo.2 AMX bacteria immobilized on a carrier
引用:和木 美代子::産環境情報, No.56, p.5(2015)
Quote:Miyoko Waki: Publication of Livestock Environment Improvement Organization, No.56, p.5(2015)
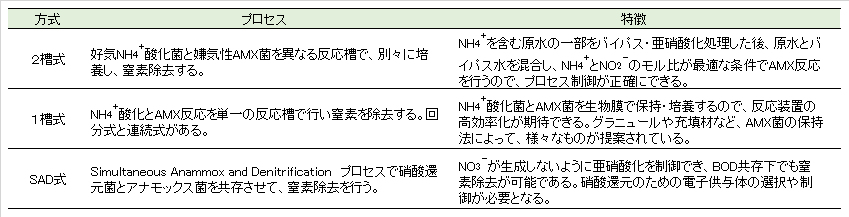
(2)AMX窒素除去プロセス
AMXを利用した窒素除去の実規模施設は、世界中で100件を越える施設が稼働しているようである。国内でも、各社から実用化プロセスが提案されている。大きく分けて、2槽、1槽およびSADの3方式がある。
(2) AMX nitrogen removal process
It seems that more than 100 full-scale facilities for nitrogen removal using AMX are in operation around the world. Even in Japan, each company has proposed a practical process. There are three main methods: 2 tanks, 1 tank and SAD.
6.3 AMXリアクター
生育の遅いAMX菌を反応槽へ保持するため、(1)グラニュール法または(2)担体固定化法が利用されている。
(1) 担体固定化法
担体としては、布・紐・スポンジ板などの固定型と流動型がある。要点は、担体と廃液との効果的な接触および窒素ガスの排出である。また、高濃度のNO2–は阻害因子であるので、反応槽内の流動方向に濃度差が生じないように廃液を循環している。また、固定型では、振動などにより、担体内表面に生成した微細なN2ガスを効率的に排出する工夫がなされている。
6.3 AMX reactors
In order to retain the slow-growing AMX bacteria in the reaction vessel, (1) granule method or (2) carrier immobilization method is used.
(1) Carrier immobilization method
As the carrier, there are a fixed type such as a cloth, a string, and a sponge plate, and a fluid type. The point is effective contact between the carrier and the effluent and the emission of nitrogen gas. In addition, since high-concentration NO2– is an inhibitor, the waste liquid is circulated so that there is no difference in concentration in the flow direction in the reaction vessel. Further, in the fixed type, a device is designed to efficiently discharge the fine N2 gas generated on the inner surface of the carrier by vibration or the like.
(2) グラニュール法
この方法は嫌気性生物処理に利用されているUASB法と同じような原理で、UASB法ではメタンガスを回収する固液気分離装置を有しているが、本法では同装置は不要である。グラニュールの育成に数十日を有するので、稼働している施設から、グラニュールを移植して立上げを速くする。
また、(1)示す流動担体型も同様な装置が利用される。
(2) Granule method
This method has the same principle as the UASB method used for anaerobic organism treatment, and the UASB method has a solid-liquid air separation device that recovers methane gas, but this method does not require this device. Since it takes dozens of days to grow granules, transplant granules from an operating facility to speed up the start-up.
A similar device is also used for the fluidized carrier type shown in 6.2(1).

写真3 AMX菌固定型リアクター Photo.3 AMX bacteria fixed reactor.
引用 Quote: https://www.life.sojo-u.ac.jp/environ/research.html

写真4 AMXグラニュール Photo.4 AMX guranules.
引用 Quote: https://www.semanticscholar.org/paper/
The-SHARON-anammox-process-for-the-treatment-of-by-Sousa/
0bad112ffb62bb90b3c7164af95a31f59c74b75e/
figure/6
6.4 アナモックス実施例
(1) 天然ガスかん水の部分亜硝酸化-アナモックス処理
関東天然瓦斯開発(株)
日本では、地下500~2,000mから高塩分の地下水を汲み上げ、天然ガスおよびヨウ素(世界生産量の34%)を回収している。資源回収排水には100~200mg/LのNH4+が含まれており、この処理に1槽型PN-AMX法を適用した技術開発を行っている。
6.4 Anammox Applications
(1) Partial nitrite treatment of natural gas brackish water - anamox treatment
Kanto Natural Gas Development Co., Ltd.
In Japan, high-salt groundwater is pumped from 500 to 2,000 m underground to recover natural gas and iodine (34% of world production). Resource recovery wastewater contains 100 to 200 mg/L of NH4+, and they are developing technology by applying the one-tank PN-AMX method to this treatment.
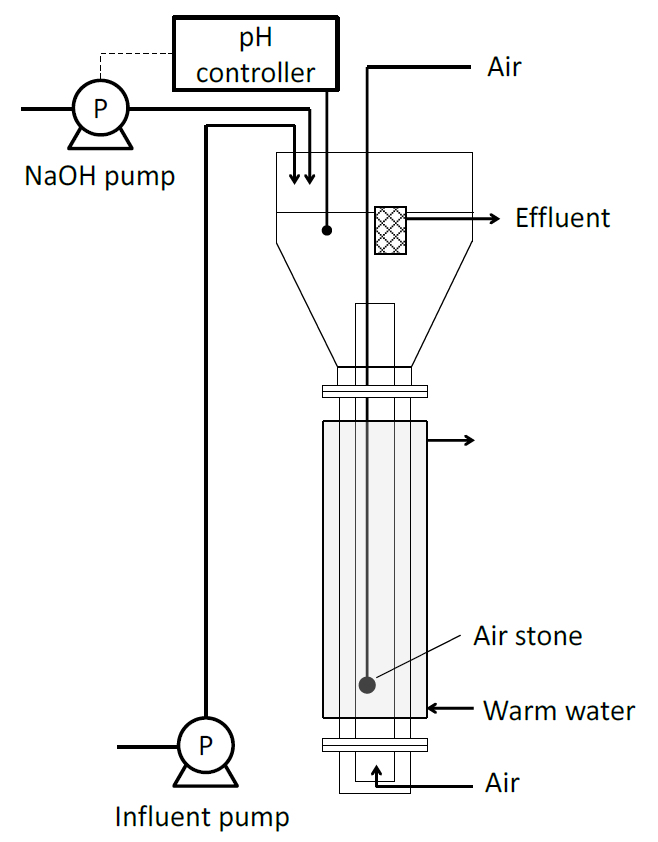
図5 PN-AMXリアクターの概略図 Fig.5 Schematic diagram of the PN-AMX reactor.
引用:横田 信之:東京農工大学・博士学位論文(2019), p.54
Quote: Nobuyuki Yokota: Tokyo University of Agriculture and Technology, Doctoral Dissertation(2019)、p.54
(2) 固定床型アナモックスプロセスによる返流水の窒素除去
(株)タクマ・熊本市上下水道局・日本下水道事業団
下水処理場での総返流水(汚泥濃縮脱離液および消化槽汚泥脱水ろ液)には、高濃度のNH4+(当実験処理場:600~700mg/L)が含まれている。この対策として、前処理-部分亜硝酸化-AMXの各工程から構成される実証プロセスの結果(90%以上の窒素除去など)を示すとともに、考察(菌叢解析など)を行っている。
(2) Nitrogen removal of return water by fixed-bed anamox process
TAKUMA Co., Ltd., Kumamoto City Waterworks and Sewerage Bureau, Japan Sewage Works Agency
The total return water (sludge concentrated desorbed liquid and digestive tank sludge dewatering filtrate) at the sewage treatment plant contains a high concentration of NH4+ (this treatment plant: 600 to 700 mg/L). As a countermeasure, the performance (90% or more nitrogen removal, etc.) of the test plant, consisting of each process of pretreatment, partial nitrite formation and AMX reaction, are shown, and considerations (bacterial flora analysis, etc.) are conducted.
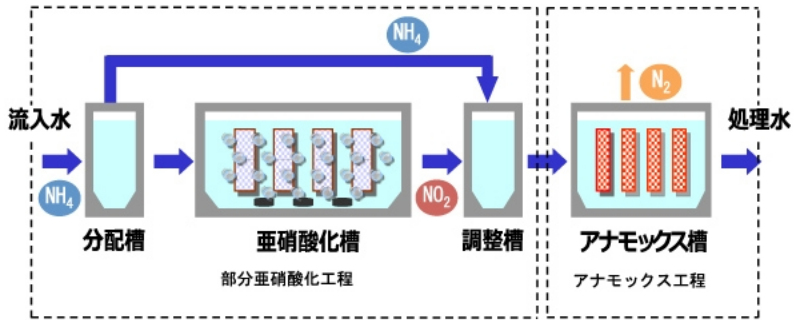
図6 アナモックスプロセスの処理フロー Fig.6 Processing flow of the anammox process.
引用 Quote:TAKUMA HP (https://www.takuma.co.jp/product/water/kodo/anammox.html)
(3) 下水の高度処理におけるアナモックス処理
(株)明電舎・神戸市建設局
電力削減および温暖化を図るため、AMXを適用した新たな下水処理施設の技術開発を実施した。本技術の特徴は、低NH4+濃度・低水温の下水にも対応できる本流処理槽と汚泥消化槽を含む各工程へAMXを導入した現場での実証実験である。
(3) Anamox treatment in advanced treatment of sewage
Meidensha Co., Ltd., Kobe City Construction Bureau
In order to reduce power consumption and global warming, they have developed technology for a new sewage treatment facility that applies AMX. The feature of this technology is a test experiment in the field where AMX is introduced into each process including the mainstream treatment tank and sludge digestion tank that can handle sewage with low NH4+ concentration and low water temperature.
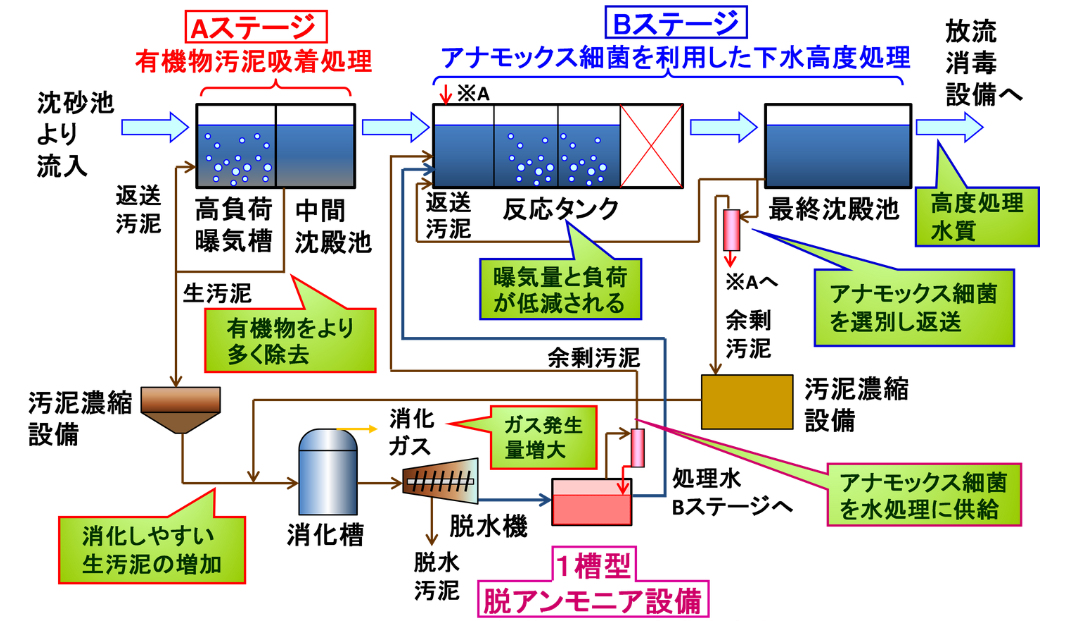
図7 アナモックス細菌を用いた高濃度窒素処理 Fig.7 High-concentration nitrogen treatment using anammox bacteria.
引用 Quote:明電舎 MEIDEN HP (https://www.meidensha.co.jp/news/news_03/news_03_01/1223555_2469.html)
6.4 アナモックス反応の実用化と科学的意義
AMX反応が発見され、その普及が期待されたが、国内では硝化脱窒法に比較すると実用化例は少ない。この理由は、新しいプロセスを立ち上げるための種汚泥を確保することが困難であった。今日、稼働プラントも増えつつあり、種汚泥の問題は解決しつつある。AMX菌の増殖速度が極めて遅く、菌体の保持・管理に高度な技術が求められ、高齢化と管理要員の不足もその理由の一つであろう。
C/N比が適切で高濃度廃水では、酸素の供給量・濃度を精密に制御できる活性汚泥法により有機物と窒素の同時除去が可能である。C/N比が低い廃水の窒素除去には、硝化・脱窒法あるいはAMX法が必要である。
AMX反応は、他の独立栄養細菌と同じく、特別な生物反応ではない。しかし、AMX菌は未だ純粋培養がなされていない。AMX菌の学術研究は自然界での窒素循環の複雑な生物学的経路を理解する上で、極めて重要な意義を有する。生活・産業廃水からの窒素除去の低コスト・汚泥化のみならず、農業における合理的な窒素管理と増産、自然現象や農業による温室効果ガスN2Oの発生削減など、今後のAMX菌に係る科学技術の進展が期待される。
6.4 Practical application and scientific significance of AMX
The AMX reaction was discovered and was expected to spread, but there are not so many practical examples in Japan as had been expected compared to the nitrification-denitrification method. The reason for this is that it was difficult to secure seed sludge to launch a new process. Today, the number of operating plants is increasing, and the problem of seed sludge is being solved. The growth rate of AMX bacteria is extremely slow and advanced technology is required for the operation of AMX process. The shortage of operation personnel with the aging population in Japan may be one of the reasons.
For high-concentration wastewater of an appropriate C/N ratio, it is possible simultaneously to remove organic matter and nitrogen with the activated sludge method that can precisely control the supply and concentration of oxygen. The nitrification-denitrification method or AMX method is required to remove nitrogen from wastewater of a low C/N ratio.
The AMX reaction, like other autotrophic bacteria, is not a special biological reaction. However, AMX bacteria have not yet been purely cultured. Academic research on AMX bacteria is of vital significance in understanding the complex biological pathways of the nitrogen cycle in nature. Science and technology related to AMX bacteria are expected to progress not only low cost and sludge removal of nitrogen from domestic and industrial wastewater, but also rational nitrogen management and production increase in agriculture, reduction of greenhouse gas N2O generation due to natural phenomena and agriculture.
The meaning of DO and its control
DO is an extremely important operating factor in a bioreactor utilizing aerobic microorganisms. Here, the meaning of DO and its control are explained in detail.
反応槽でのDOの挙動
DOの話の前に、収入と預金量の話をする。収入が多いから、預金量が多いとは限らない。振込量と引出量の差が預金量となる。
ここで好気性生物反応槽では、振込量が酸素供給量、引出量が酸素消費量、預金量がDO(正確には、DO[mg/L=g/m3]×反応器容積V[m3])ということになる。
酸素供給量>酸素消費量の場合にはDOは平衡状態まで上昇するし、酸素供給量<酸素消費量の場合にはDO = 0となる。
酸素消費量は、生物量(正確には、生物による有機物の最大分解速度)>有機物量(正確には、有機物の負荷量)の場合には有機物流入量が律速になり、生物量<有機物量の場合には生物の呼吸量が律速となる。
なお、酸素供給が曝気により行われる場合には、その供給量は気液界面での酸素の移動速度(溶解速度)によるが、これは気液界面の総面積(曝気の送風量と気泡径などに依存)、酸素分圧、飽和DOと溶存DOとの差など多くの因子の関することとなるので、別のページで記載することとし、ここでは触れないこととする。
Behavior of DO in the reaction tank
Before talking about DO, talk about income and deposit. Because of high income, deposit is not always high. The difference between the transfer and the withdrawal is the deposit.
Here, in the aerobic biological reaction tank, the transfer is the oxygen supply, the withdrawal is the oxygen consumption, and the deposit is DO (to be precise, DO [mg-O2/L = g-O2/m3]×reactor volume V[m3]).
When oxygen supply > oxygen consumption, DO rises to the equilibrium state, and when oxygen supply < oxygen consumption, DO decreases to “0”.
Oxygen consumption depends on the following two factors. (1) The amount of inflow organic substances becomes the rate-determining factor, when the amount of organisms (to be exact, the maximum decomposition rate of organic substances by organisms) is more than the amount of organic substances (to be precise, load of organic substances). (2) The respiration rate of living organisms is rate-determining, when the amount of living organisms is less than the amount of organic substances.
When oxygen is supplied by aeration, the amount of oxygen supply depends on the transfer velocity (dissolution rate) of oxygen across the gas-liquid interface. This depends on the total area of the gas-liquid interface (aeration air flow rate and bubble diameter, etc.). It depends on various factors), oxygen partial pressure, difference between saturated DO and dissolved DO, etc., so it will be described on another page and will not be discussed here.
DOの制御
呼吸器(肺や鰓など)・血液などの酸素取込・運搬系および呼吸を行う体細胞から構成される水生動物と水浄化の微生物の主役である単細胞菌(懸濁培養系では微生物フロック、または担体付着系では生物膜)においては、最適な水中DO値が全く異なるので注意する。水生動物では鰓で酸素交換を行うので外部DO値が重要となるが、単細胞では酸素が細胞膜を通過して細胞内へ直接取り込まれる(濃度差による分子拡散)。
したがって、生物反応でのDOは上述したように、酸素供給量と酸素消費量のバランス(過不足)の指標と考えるべきで、DO値そのものに特に拘る必要はない。好機生微生物の反応槽では、数mg/Lに設定する。1mg/L以下では、DO計の校正や維持管理(センサへのスラムの付着など)が不適切であル場合やDO測定への妨害物質(酸素センサーの隔膜を通過する分子状電子供与体)が共存する場合には、DOが本当に酸素供給量が不足状態であるかどうか判定ができない。
一般的に反応槽の好気性微生物で重要なことは、その槽内におけるDO値の位置分布が重要となる。反応槽の容積が大きくなるほど、有機物(反応中間体を含む)濃度の位置分布が異なり、DO値分布も異なる。反応槽内の汚水流動状態から見ると反応槽も混合型から層状流型まで様々である。流入部、中央部、流出部でのDO値は異なり、流出部でのDO値がゼロ近傍では酸化分解が不完全であることを示している。
目次へ
DO control
Note that optimal DO values in water are quite different for large multicellular organisms and microorganisms. For example, in aquatic animals, oxygen is supplied to somatic cells by oxygen uptake and transport by the respiratory system (lung, gills, body surface, etc.) and blood. On the other hand, in single-celled bacteria, which is the main role of water-purifying microorganisms, oxygen passes through the cell membrane and is directly supplied to cells (molecular diffusion due to a difference in concentration)..
Therefore, DO in the biological reaction should be considered as an index of the balance (excess or deficiency) of the oxygen supply amount and the oxygen consumption amount, as described above, and it is not necessary to be particularly concerned with the DO value itself. In the reaction tank for aerobic microorganisms, DO is set to several mg/L. Below 1 mg/L, it is not possible to determine whether DO is really in an insufficient oxygen supply, in the case of
incorrect calibration and maintenance of DO meter (such as adhesion of slum to the sensor) or coexistence of interfering substances (molecular electron donor passing through oxygen sensor membrane) to DO measurement.
Generally, what is important for aerobic microorganisms in a reaction tank is the spatial position distribution of DO values in that tank. The larger the volume of the reaction tank, the different the position distribution of the concentration of organic substances (including reaction intermediates) and the DO value distribution. Furthermore, when viewed from the flow state of sewage in the reaction tank, the reaction tank also varies from a mixed type to a laminar flow type. The DO values at the inflow part, the central part, and the outflow part are different, indicating that the oxidative decomposition is incomplete when the DO value at the outflow part is near zero.
To table of contents
参考文献
1) 河村 清史(監修)、2013:浄化槽工学、pp.85-89、日本環境整備教育センター
2) 楠井 隆・松原 数喜、2007:廃水処理施設における硝化細菌と硝化能力の関連、富山県立大学紀要、Vol.27、pp.93-97
3) 鈴木 孝仁・他、2014:新生物-生物基礎・生物、数研出版、p.428
4) 野村 祐次郎・他、2016:新化学-化学基礎、数研出版、p.340
5) 芳倉 太郎・西尾 孝之・福永 勲、1999:生物学的硝化脱窒芳による高度処理、生活衛生、Vol.43、No.21、pp.49-64
6) 吉村 二三隆・北川 幹夫、2011:わかりやすい水処理設計、技術評論社、pp.83-89
目次へ
References
1) Kiyoshi Kawamura (eds.), 2013: Septic tank engineering, pp.85-89, Japan Education Center of Environmental Sanitation.
2) Takashi Kusui, Kazuki Matsubara, 2007 : Related of nitrifying bacteria and nitrification capacity in the waste water treatment facility, Bulletin of Toyama Prefectural University, Vol.27, pp.93-97
3) Takahito Suzuki et al., 2014 : Neo-Biological Biology/Biological Sciences, Suken Shuppan, p.428
4) Yujiro Nomura et al., 2016 : New Chemistry-Chemical Fundamentals, Suken Shuppan, p.340
5) Taro Yoshikura, Takayuki Nishio, Isao Fukunaga, 1999 : Advanced treatment by biological nitrification and denitrification, Seikatu Eisei (published by Osaka Food Hygiene Association), Vol.43, No.21, pp.49-64
6) Fumitaka Yoshimura, Mikio Kitagawa, 2011: Easy-to-understand water treatment design, Gijutsu-Hyohron, pp.83-89
Note: References 1) to 6) are all written in Japanese.
To table of contents
掲載:2017年09月22日
更新:2017年11月19日(再曝気槽に関する記述を訂正)
更新:2020年06月14日(英語版追加)
更新:2021年01月29日(Anammox法を追加)
Publication date: September 22, 2017
Update: November 19, 2017 (Correction about re-aeration tank)
Update: June 14, 2020 (English version added)
Update: January 29, 2021 (Anammox process added)
